|
健亞生物科技股份有限公司(健亞)成立於1993年,位於台灣新竹科學工業園區,是台灣第一家獲得行政院國發基金投資的生技製藥公司。我們專注於小分子新藥的研究開發,並結合海內外先進科技與人才,以創新技術打造高品質藥品,提升國際競爭力,為全球患者提供更安全有效的醫療選擇。 |
|
健亞生物科技股份有限公司從事研究與開發小分子藥物。公司的願景為希望成為以開發”Niche in class”新藥為主的特色藥廠,生產合理價格的高品質藥物行銷國際,嘉惠病患,創造股東利益。公司的策略為結合海內外專家、業者以及政府力量,開發風險均衡的產品組合,使公司穩健成長中保留躍升機會。 |
|
健亞具有最廣泛的新藥開發能力與經驗,從原料藥生產到人體臨床試驗,從藥物篩選到美國FDA新藥審批。隨著國內新藥開發環境逐漸成熟,健亞逐漸將若干原有能自己執行的工作(如藥物合成、生化分析、人體PK試驗)轉為委外執行。但唯有充分瞭解該項技術的細節,才能保證委外工作的品質與效能。因此健亞廣泛的新藥開發技術與經驗,成為藥物開發重要的競爭優勢,也形成本公司技術/產品的特色,即在於可廣泛開發各種類型藥物,從最困難複雜的新成分新藥、改良劑型新藥、緩釋劑型新藥,到特色學名藥。健亞的另一項優勢在於曾經執行過相當多的政府計劃,建立了良好的計劃執行能力、專案管理能力,以及各種產、官、學、研單位的良好互動。健亞在2012年上櫃後,亦展開一系列的策略投資,成功的引進具國際競爭優勢的合作夥伴如浩宇生醫、華宇藥品及美國Soleno。 |
|
健亞擁有完整的新藥開發能力,從藥物篩選、原料藥生產到人體臨床試驗,再到美國FDA新藥審批,確保藥品符合全球市場標準。我們的策略包括:■ 新成分新藥:透過產業聯盟與政府補助,完成早期人體臨床試驗,後續授權國際夥伴進一步開發。■ 新途徑與新劑型新藥:優先完成國內查驗登記,並拓展國際市場。■ 特色學名藥:專注於突破專利與劑型限制,開發具競爭力的學名藥品。透過這些策略,健亞致力於研發價格合理、品質卓越的藥品,並行銷至全球市場,以造福病患並創造股東價值。 |
|
健亞深知新藥開發對生產設備與品質管理的嚴格要求,因此投資購買原必治妥施貴寶(Bristol-Myers Squibb)GMP廠,並持續升級其設備與管理標準。我們嚴格遵循美國FDA的cGMP標準,並已獲得:■ 台灣衛生署GMP確效認證(2004年)■ 日本厚生省醫藥品外國製造業者認定許可(2007年)■ PIC/S GMP國際標準認證(2010年)這些認證不僅確保我們的產品符合全球藥品品質標準,也讓健亞成為眾多國際藥廠(如第一三共、羅氏等)在台灣的指定代工夥伴。 |
|
健亞的業務團隊積極拓展市場,除了行銷自有產品外,也透過策略聯盟強化業務能力。我們的銷售通路涵蓋:■ 台灣市場:醫學中心、區域醫院、地區醫院及診所。■ 海外市場:自2001年起拓展東南亞市場,並與歐美藥廠合作,引進國際級產品。此外,我們透過策略投資與聯盟,如與浩宇生醫、華宇藥品及美國Soleno等夥伴合作,強化國際競爭力,推動台灣生技產業向全球市場邁進。 |
公司沿革
1995 |
行政院開發基金投資,成為第一家政府支持的指標性生技新藥公司。 |
1997 |
購入原必治妥施貴寶 GMP 工廠,完成臨床試驗部門之建立、引進 CRO 業務。 |
2000 |
治療 SLE 用藥 PrestaraTM 完成臨床III期試驗,向美國FDA申請新藥審查(NDA),並於2002年獲美國 FDA “Approvable Letter” 。 |
2001 |
與 Roche 合作,開發/生產抗病毒用藥 Ribavirin。 |
2003 |
新藥「欣沛方」(紫杉醇針劑)、「優合」(尿失禁治療藥)上市。 |
2003 |
登錄為興櫃交易公司,首年損益兩平。 |
2004 |
授權日本 Tanabe 及韓國 Yuhan 開發 PrestaraTM,收取先期權利金。 |
2008 |
與國衛院合作,共同開發抗糖尿病新藥 DBPR108 。中國市場授權石藥集團(2012) 。 |
2009 |
與台灣第一三共簽 代工 合約。 |
2010 |
工廠通過衛生署 PIC-S/GMP 認證。核准新增無菌眼用液劑製造(2014) 。 |
2012 |
上櫃掛牌於櫃買中心(股票代號:4130)。 |
2013 |
轉投資心悅 。協助CMC,完成SND11與 SND13 (2014)美國 IND filing,進入臨床Ⅱ/Ⅲ 期。 |
2013 |
轉投資瑞寶(股票代號:6479)與生控,取得HPV Vx中國市場共同開發權利。 |
2014 |
PMR 臨床Ⅱ期結果符合預期。亞太地區授權給日本Otsuka藥廠,共同開發。 |
2014 |
Granpatch 進入登記用臨床試驗。 |
2015 |
清腸劑 Bowklean獲得TFDA批准。PMR進入臨床Ⅲ 期。 |
2015 |
轉投資美國細胞免疫治療公司 Medeor 。 |
2016 |
轉投資浩宇NaviFUS ,以非侵入性聚焦超音波短暫打開血腦屏障,
|
2017 |
轉投資Soleno,研發治療小胖Willie(PWS)疾病的新藥。
|
2017 |
PMR完成美國IND申請,正式啟動在美國的人體試驗。 |
2018 |
獲得TFDA核准治療狼瘡腎炎新藥 Mycocep。 |
2019 |
PMR完成美國樞紐性臨床試驗。 |
2019 |
與浩宇共同投資GNI,啟動NF02治療阿茲海默症創新醫材計畫於澳洲墨爾本。 |
2020 |
PMR完成美國Pre-NDA會議,GV17申請Pre-IND會議。治療糖尿病新藥DBPR108於中國大陸進入第三期臨床試驗。PMR取得中國大陸專利。 |
2022 |
新藥GX17開發用於治療「抗磷脂症後群」適應症,通過美國FDA審查,獲准進行首次人體臨床試驗。 |
經營團隊
職 稱 |
姓 名 |
主 要 經 (學) 歷 |
目前兼任其他公司之職務 |
董事長兼策略長 |
陳 正 |
美國羅徹斯特大學化學博士諾華計劃主持人Genelabs亞洲業務副總裁華鼎生技顧問(股)公司董事長行政院生技產業策略諮議委員會(BTC)委員 |
昌達生化科技(股)公司 法人代表(董事)Genovate Biotechnology(Cayman) Co., Ltd. 法人代表(董事)華宇藥品(股)公司 董事長兼策略長瑞寶基因(股)公司 法人代表(董事)浩宇生醫(股)公司 法人代表(董事長)兼策略長Genovate NaviFus (Australia)Pty.Ltd.法人代表(董事)松瑞製藥(股)公司 法人代表(董事) |
總經理 |
朱佳真 |
美國哈佛大學醫療政策與管理碩士健亞生物科技股份有限公司國際事務處長健亞生物科技股份有限公司新藥開發事業副總經理 |
華宇藥品股份有限公司 法人代表(董事)浩宇生醫股份有限公司 法人代表(董事)Genovate NaviFus Inc.法人代表(董事)Genovate NaviFus (Australia)Pty.Ltd. 法人代表(董事) |
財務副總經理 |
林惠玲 |
交通大學財務金融研究所碩士眾信會計師事務所副組長健亞生物科技股份有限公司稽核經理健亞生物科技股份有限公司財務處長 |
– |
行政處資深處長 |
蔣維民 |
師範大學生物研究所碩士友嘉實業(股)公司管理副理道生教育機構人事主任 |
– |
廠長 |
黃光亮 |
世新 印刷攝影科畢寶齡富錦 生產課長瑞安大藥廠 副廠長 |
– |
企業社會責任
推動永續發展執行情形及與上市上櫃公司永續發展實務守則差異情形及原因
推動項目 |
執行情形 |
與上市上櫃公司永續發展實務守則差異情形及原因 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
是 |
否 |
摘要說明 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
一、公司是否建立推動永續發展之治理架構,且設置推動永續發展專(兼)職單位,並由董事會授權高階管理階層處理,及董事會督導情形? |
V |
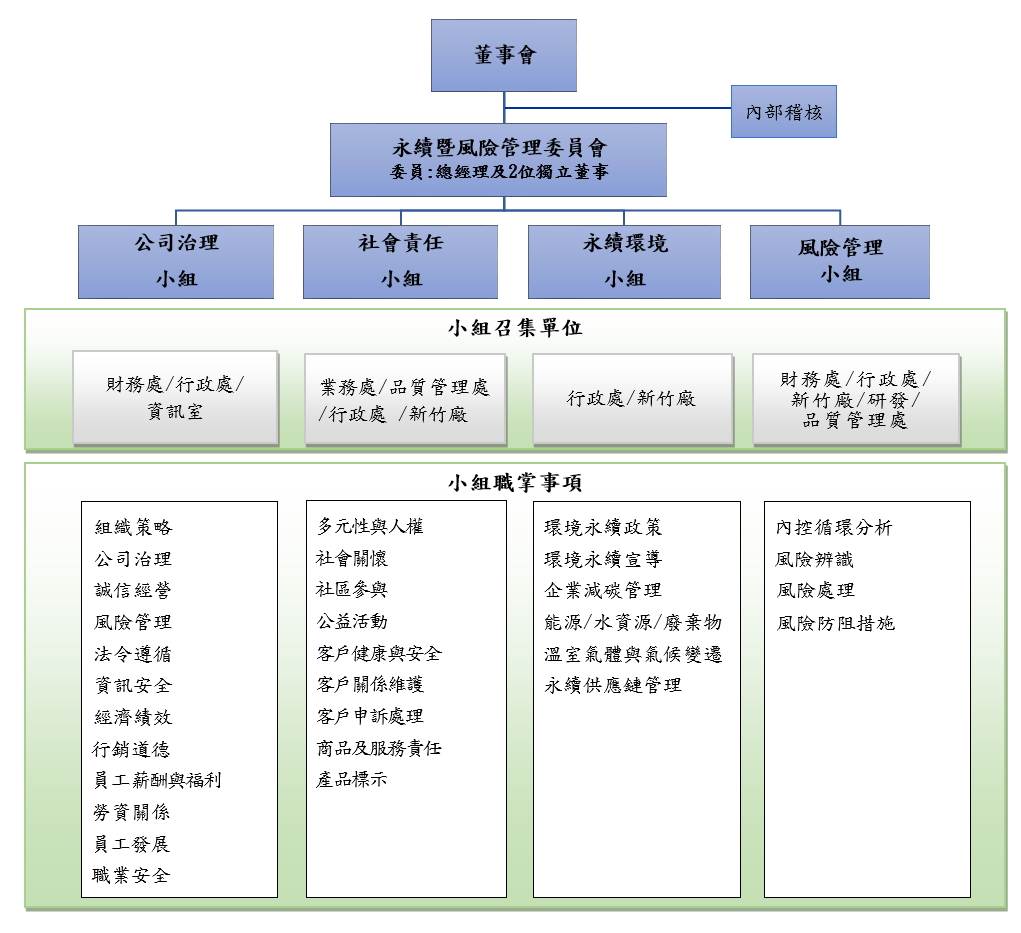
本公司於113年08月召開董事會,通過「永續暨風險管理委員會組織規程」,正式設立董事會層級之「永續暨風險管理委員會」,於113年08月06日並委任蘇來守、張金明2位獨立董事及兼任公司總經理之朱佳真董事,蘇來守董事已於114.11.05辭任。另於114年11月27日補行委任李世仁、劉克宜2位獨立董事,組成該委員會成員(共4名委員其中1位為董事及3位為獨立董事),負責督導企業永續策略方向、年度計畫、執行成效等。並至少一年一次向董事會報告。董事會督導及推動情形:本公司董事會定期追蹤溫室氣體盤查及查證管控執行進度,113年於11月05日董事會訂定「永續資訊管理作業辦法」、「永續報告書編製及確信之作業程序」。有關永續發展推動情形由「永續暨風險管理委員會」責成經營團隊擬訂年度計劃推動,並定期提報董事會。114年08月05日「永續暨風險管理委員會」通過「民國114年風險評估與執行情形報告」及「民國114年(2025)永續發展推動計畫案」,永續發展推動計劃共有3面項:˙環境面包含節能減碳、氣候變遷。˙社會面包含利害關係人、社會及社區服務。˙公司治理面包含誠信永續、法令遵循。並於114年08月05日董事會通過。由總經理親自督導各部門,依部門職掌下設「公司治理」、「社會責任」、「永續環境」、「風險管理」四小組,負責永續及風險管理相關事務之推動。其範疇從員工照顧、健康職場、環境保護、產品責任到投資人權益、公益捐贈…均戮力朝永續發展、善盡社會責任之目標邁進。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
二、公司是否依重大性原則,進行與公司營運相關之環境、社會及公司治理議題之風險評估,並訂定相關風險管理政策或策略? |
V |
本公司於113年08月由董事會通過訂定「風險管理政策與作業程序」,明訂風險管理之組織架構與權責及其風險辨識、分析、評價、回應及監督之作業程序,以作為各單位風險管理之最高指導原則。風險管理組織架構與權責:
各單位依重大性原則,考量經濟、環境、社會面等公司治理議題對客戶、投資人及其他利害關係人可能產生重大影響者,進行風險評估,茲整理營運面5項、財務面2項、研發面3項、資訊面2項、人資面1項及環境面2項,共計15項之風險項目。並擬訂因應策略,併同執行情形匯整報告,提報「永續暨風險管理委員會」審議,並經114.08.05董事會討論通過。本公司風險評估邊界為健亞生物科技股份有限公司(含主要營業據點,但不包含以投資目的而成立的子公司)。114年度風險評估與執行情形:
|
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
三、環境議題(一)公司是否依其產業特性建立合適之環境管理制度? |
V |
本公司於PIC/S GMP規範下從事製藥作業,依循環保署環境管理系統標準,制定各項生產作業與環境保護規範,推行各項污染防治及資源節約工作。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(二)公司是否致力於提升能源使用效率及使用對環境負荷衝擊低之再生物料? |
V |
本公司各項研發及製程尚無使用對環境負荷衝擊高之物料,並已嚴格實施垃圾分類及紙張回收再利用措施,致力提升資源利用效率。目前主要的能源消耗來自於廠區機台用電、工作場域之照明及空調用電,為達成低碳營運之長期目標,健亞預計於114年起推行節能方案,包含盤點及汰換廠區老舊高耗能機台、更換廠區照明為節能 LED、更新老舊空調設備等措施。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(三)公司是否評估氣候變遷對企業現在及未來的潛在風險與機會,並採取相關之因應措施? |
V |
由「永續暨風險管理委員會」督導,總經理帶領經營團隊評估氣候變遷對企業營運、現在及未來潛在風險與機會的盤點,執行溫室氣體排放量、用水量及廢棄物總重量之統計,並制定節能減碳、溫室氣體減量,減少用水或其他廢棄物管理之政策。遵循法規,加強能源管理與資源再利用等因應措施,據以推動以降低公司營運活動對氣候變遷之衝擊。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(四)公司是否統計過去兩年溫室氣體排放量、用水量及廢棄物總重量,並制定溫室氣體減量、減少用水或其他廢棄物管理之政策? |
V |
為降低環境污染,本公司已將鍋爐之燃料以對環境污染的衝擊較小之天然氣取代污染性風險較高之重油,並頒佈「工作場所行為規範」,要求節約用水用電之生活習慣養成,期能節約能源。本公司持續統計溫室氣體、水及廢棄物等環境資訊,並且每年揭露於公司網站及永續報告書中。盤查範圍為健亞生物科技股份有限公司(含主要營業據點,但不包含以投資目的而成立的子公司),因此與合併財務報告中個體不同。113年度起每年進行公司的溫室氣體盤查,依循GHG protocol準則,以營運控制法鑑別排放源,並採用最新的IPCC全球暖化潛勢(Global Warming Potential, GWP)資料進行統計,113年相關盤查作業已經過第三方查證,確保數據的品質及完整性。
隨著近年極端氣候加劇,全球降雨分布不均情況已成常態,暴雨、乾旱、洪水之發生頻率與嚴重程度逐年突破過往紀錄,不僅對一般民生用水造成影響,同時也使企業之供應鏈供貨不穩定性、廠區營運中斷風險提升,為了因應未來可能面對的缺水挑戰,我們致力於推動良好的水資源管理。113年鑑別結果顯示本公司全據點皆未坐落於高水資源壓力區域,未來將持續逐年追蹤評估各據點之水資源壓力,避免公司鄰近居民及生態造成潛在衝擊。112年及113年總取水量分別為31.958百萬公升及32.792百萬公升。為避免自身營運之廢棄物對鄰近社區及生態造成負面衝擊影響,我們建立廢棄物清運與管理措施,並透過清除處理廠商之GPS 系統追蹤廢棄物清運車輛之運送軌跡,以確保事業廢棄物皆被妥善處置。114年度本公司持續針對合作之廢棄物清除處理廠商進行文件審查與系統監控,未發現清除處理廠商有任意傾倒或其他違規事項。未來將持續加強監管機制,以維持廢棄物0違規之目標。
公司持續統計溫室氣體排放量、用水量及廢棄物總重量。113年溫室氣體排放量、112年及113年廢棄物總重量已完成第三方查證,114年之資訊截至年報刊印日止仍在進行查證中,最新資訊可參閱本公司網站及永續報告書。此外,本公司113年已購置一台能源效率第2級冰水主機總價16萬元。透過調整設備使用頻率以提升能源使用效率,有效實現節能減碳,預估冰機可節電2,474KW /年,半成品室可節電34,629KW/年。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
四、社會議題(一)公司是否依照相關法規及國際人權公約,制定相關之管理政策與程序? |
V |
本公司依相關勞動法規制定各項內部管理辦法;尊重國際公認之基本勞動人權原則,雇用條件排除性別、年齡、宗教、性向等因素;無雇用差別待遇。保障員工之合法權益。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(二)公司是否訂定及實施合理員工福利措施(包括薪酬、休假及其他福利等),並將經營績效或成果適當反映於員工薪酬? |
V |
(1)本公司標舉人性之管理模式,對員工權益及勞資關係和諧極其重視,無論出勤、薪資、保險、退休,均依關法令執行,其中加班費,勞保自付等項目,甚而優於勞基法規範。公司每年均進行員工滿意度調查及優質之健康檢查,對員工之身心健康,職涯發展及自我實現均由人資部門審慎管理規劃。勞資關係良好。(2)本公司章程第二十八條之一明訂公司應以當年度獲利狀況不低於百分之十分派員工之酬勞,114年配發員工酬勞新台幣1,529仟元。(3)本公司訂有「員工酬勞辦法」、「業績獎勵辦法」、「績效考核辦法」及「員工獎懲辦法」,將薪酬與考核及獎懲結合。本公司依各項營運指標達成率,及時發放績效獎金,112年、113年及114年各發放新台幣13,383仟元、11,783仟元及7,631仟元之績效獎金,以獎勵全體同仁開創業績之貢獻。(4)本公司連續三年,均參考通貨膨脹指標,調升同仁薪資。111年調幅3.3%,112年調幅3.3%及113年調幅4.0%。(5)本公司行政處於114年11月執行該年度全體員工滿意度調查,以了解組織氣候,並針對重大問題進行深度溝通和訪談與訂定改善計畫。本次員工意見調查內容包括工作滿意度、溝通、薪資與福利、員工發展、經營管理、績效管理、團隊合作精神、品質觀念、工作環境及公司形象等10個構面,共29項指標。
|
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(三)公司是否提供員工安全與健康之工作環境,並對員工定期實施安全與健康教育? |
V |
(1)本公司設置安全衛生管理單位,並設有合格證照之安全衛生主管人員,依法令規定制定工作場所消防防護計劃,定期執行消防安全設備檢修作業及公共建築物防火避難設施與設備安全檢查,並向主管機關申報。公司各出入口亦設有門禁管制、電梯等公共設施定期保養,設有保全人員及架設監視器等,維護工作場所安全及保障所有員工的人身安危。本公司114年無火災情事發生。(2)生產作業環境中主要特別危害源:噪音作業、粉塵作業、特化作業及有機溶劑,制定作業規劃相關危害預防措施,於從事特殊職務包含有機、特化與可能噪音之作業員工,除提供作業時所需之個人防護具(包括口罩、手套、安全護目鏡及實驗衣)外,亦嚴格要求作業前須配戴完整之個人防護具,並須於抽氣櫃/抽氣罩下處理有機溶劑、特定化學品,噪音危害之預防,提供耳塞/耳罩供同仁於有感之噪音作業場所中使用,並於每年定期舉辦噪音、粉塵及特殊化學品健檢。本公司114年皆未有重大違規情事,亦未發生職業災害。(3)本公司全額投保團體保險(擴及配偶及子女),照顧員工身體健康;也透過福委會,舉辦各式活動。本公司標舉人性化管理,致力提供員工一個身心靈健康平衡的工作環境。(4)本公司每年舉辦健康檢查,體檢檢查結果由特約護理師及職業醫學科專科醫師實施衛教及健康追蹤檢查,必要時應實施疑似工作相關疾病之現場評估。特約醫護亦定期到廠諮詢服務,辦理健康管理、職業病預防及健康促進等勞工健康保護事項。(5)本公司每年舉辦1至2次安全、衛生、消防及緊急應變等訓練,並舉辦員工成長營,公司董事亦定期參與課程,落實有關社會責任之教育訓練與活動。(6)本公司於110年元月獲衛福部國民健康署頒發「健康職場認證-健康啟動標章」,112年完成展延。致力創造一個健康與安全之職場環境。(7)本公司於109年間公告宣示「禁止工作場所職務遭受不法侵害之書面聲明」,由總經理親自簽署,以示決心,並公布暴力危害預防申訴管道之專線電話與電子信箱。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(四)公司是否為員工建立有效之職涯能力發展培訓計畫? |
V |
為使員工與公司同步成長,本公司透過內、外部訓練增進員工工作技能,提升工作績效,改善產品及服務品質,創造員工個人與組織整體競爭力。主管共識營:為凝聚團隊共識與強化領導效能,公司特別舉辦「主管共識營」,對象為中階主管。課程內容涵蓋策略思維、組織領導、跨部門協作及溝通管理等主題。透過主題式討論、經驗分享促進跨部門溝通與協作,活動旨在協助主管深化對公司策略方向與經營目標的理解,並持續提升領導管理及決策執行能力,強化整體組織競爭力。113年度參與主管共識營共計47人,受訓總時數為329小時。外訓/內訓:由各部門主管依業務發展或職能需求,遴選適任人員參加國內專業機構舉辦之訓練課程,相關進修費用由公司全額補助,以持續精進專業知能並強化組織競爭力。114年度員工參與外訓共計95人次,受訓總時數為696.5小時。GMP教育訓練:主要涵蓋藥品良好製造規範的基礎概念、文件與紀錄保存、變更管制及偏差處理等實務操作;同時包含製程與設備管理、設施驗證、清潔維護及環境控制,確保生產過程符合規範要求。114年11月17日參與GMP教育訓練共計116人次,受訓總時數為116小時。新進人員訓練:為協助新進人員迅速熟悉生產流程與作業標準,公司規劃完整的新人訓練課程。訓練內容涵蓋基本安全守則、機台操作、品質檢查要點及標準作業流程(SOP),藉由系統化的培訓安排,建立良好的工作習慣與職場認知。114年度工廠新進人員訓練共計15人次。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(五)針對產品與服務之顧客健康與安全、客戶隱私、行銷及標示等議題,公司是否遵循相關法規及國際準則,並制定相關保護消費者或客戶權益政策及申訴程序? |
V |
(1)本公司為符合國際標準之PIC/S GMP工廠,產品銷售及標示均符合國內外法規規定。(2)本公司訂有客訴處理程序,由品保單位專人負責,保障消費者權益。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(六)公司是否訂定供應商管理政策,要求供應商在環保、職業安全衛生或勞動人權等議題遵循相關規範,及其實施情形? |
V |
(1) 本公司訂有供應商管理程序,對上下游廠商均訂有嚴格之品質標準及稽查評估程序,提供安全、質優之產品,並藉前往主要供應商實地查核,勘驗有關環保、職安、勞動人權等規範實踐,落實共同提升企業之社會責任。本公司進行新進供應商篩選時,留意該廠商過去有無影響環境與社會之紀錄,並要求簽署「供應商自我評估表」進行審核。針對新供應商,原料藥須具有PIC/S、EDQM、WHO..等TFDA認可核發單位核發之GMP文件,依原物料適用性評估表進行確認,若原料品符合製造需求,將進一步就供應商基本情況進行相關評估作業。並於採購前簽署「品質合約書」,經由變更管制程序確認相關事項執行,變更管制文件結案前完成評估報告,審核判定適用則納入合格供應商名冊。(2)本公司針對主要供應商合約研議加註違約賠償及解約項目,如供應商原料違法使用添加物或摻雜法律禁止使用之成分,即為背信行為,本公司將依法請求賠償損失,並終止契約,不再合作。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
五、公司是否參考國際通用之報告書編製準則或指引,編製永續報告書等揭露公司非財務資訊之報告書?前揭報告書是否取得第三方驗證單位之確信或保證意見? |
V |
本公司已編製永續報告書,依循全球永續性報告協會(Global Reporting Initiative, GRI)於2021年公布之GRI通用準則2021(GRI Standards 2021)進行編製,並遵循「上櫃公司氣候相關資訊」及「上櫃公司編製與申報永續報告書作業辦法」,揭露永續相關作為。本報告書部份資訊業係委任資誠聯合會計師事務所(PwC)按照中華民國會計研究發展基金會發布之確信準則3000號「非屬歷史性財務資訊查核或核閱之確信案件」執行有限確信。確信報告請參閱本公司永續報告書。 |
尚符合守則之規範 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
六、公司如依據「上市上櫃公司永續發展實務守則」定有本身之永續發展守則者,請敘明其運作與所定守則之差異情形:本公司已於113年08月訂定公司永續發展實務守則,公司一向秉持「體貼國人健康」,回饋社會的理念,充實公司發展,謀股東最大利益。對投資股東,皆依據相關法規揭露公司重大訊息、財務資訊,董事會亦正常運作,引導公司經營策略,並有效監督經營團隊之管理功能,達成創造股東財富,公司永續經營之目標。目前營運皆遵循相關法規,尚無顯著差異。 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
七、其他有助於瞭解推動永續發展執行情形之重要資訊:(一)本公司於114年積極投入社會公益活動,10月與新竹縣湖口鄉鳳凰社區發展協會合辦「愛心捐血」活動,員工及眷屬共計40人參與,當日共募集愛心血液140袋,展現企業關懷精神與回饋社會的具體行動;12月則與新竹縣卓越志工服務協會合作辦理關懷失智老人牙醫義診活動,投入志工服務共計54人時,持續以實際行動落實企業社會責任。(二)本公司位於新竹工業區內,積極參與廠區聯誼會、教育訓練及各項之文康活動,並對公益團體、消防單位、科技學術基金會、慈善事業或藝文活動量力贊助,期能對社會略盡棉薄之力。本公司於114年10月捐贈新竹縣消防局「Cyanokit氰化物解毒劑」,成為全國第一個正式取得並配備氰化物解毒劑的消防機關,為火場救護再添一層關鍵保障。(三)本公司設有專責單位處理客戶訴願,具體回覆追蹤改善,以保護消費者權益。(四)本公司依章程已為董事、監察人及經理人投保責任保險,保障投資人權益。(五)本公司聘雇政策無性別、種族、年齡、婚姻與家庭等差別待遇。落實報酬、雇用條件、訓練與升遷機會之平等。(六)本公司本於誠信、共榮之經營理念,視員工為重要資產,除有具競爭力的薪資結構,亦有高比例公司盈餘分享員工,並有庫藏股、績效獎金、員工旅遊等獎酬措施,勞資同心協力,共創榮景。(七)多元平權的職場兩性平權健亞生技在員工職涯發展重視兩性實質平等,並納入性別多元化的考量,在人才招募、育才、留才皆不因員工性別而有差異對待。114年全體職員男性與女性之人數比為53%:47%,整體管理職男性與女性主管佔比為59%:41%,本公司總經理、財務副總均為女性,於決策階層佔重要比例。在員工發展落實兩性實質平等,給予穩定的工作環境及保障。114年男性董事與女性董事之人數比為57%:43%。禁止騷擾與歧視公司嚴格禁止任何形式的騷擾、性騷擾、歧視與恐嚇行為。為保障員工平等工作權利,並採取適當的預防、糾正、懲戒及處理改善措施,本公司訂有「道德行為準則」與「性騷擾防治措施、申訴及懲戒辦法」。員工可透過專線、電子信箱等多元申訴管道提出申訴。若涉及性別歧視或性騷擾事件,公司將成立性騷擾申訴處理委員會,以保密方式處理申訴,並以不公開方式進行調查,保護當事人的隱私及權益。依個案當事人有輔導或醫療等需要者,本公司得依申請協助轉介至專業輔導或醫療機構。並於109年間公告宣示「禁止工作場所職務遭受不法侵害之書面聲明」,由總經理親自簽署,以示決心,並公布暴力危害預防申訴管道之專線電話與電子信箱。為落實公司禁止騷擾與歧視政策,公司每年至少安排一次人權相關的教育訓練,涵蓋平等、不歧視的要求。114年無歧視及性騷擾情事發生●員工結構: ●性別比例:
●從業員工
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
勞資關係
(一)本公司各項員工福利措施、進修、訓練、退休制度與其實施情形,以及勞資間之協議與各項員工權益維護措施情形:
1.員工福利措施主要項目與其實施情形:
(1)保險
本公司員工均參加勞工保險(勞保自付額亦由公司付費),全民健康保險及團體保險(醫療險、癌症險擴及配偶子女,公司負擔全額保費納保)。
(2)健康檢查與保健促進
每年全體員工實施全身健康檢查(檢查內容包括血液常規檢查,尿液常規,癌症篩檢,X光,心電圖,腹部超音波…等),亦實施過勞量表與心理健康量表調查 並請檢驗單位醫師解說健檢內容,追蹤複檢。
109年起簽訂特約醫師及護理師,定期到場辦理健康管理,職業病預防及健康促進等勞工健康保護事項。
(3)職工福利委員會
職工福利委員會提供員工三節禮金、生日禮金、婚喪生育補助、住院急難救助及國內外旅遊及社團等活動之補助。
(4)加班給付
優於勞基法的加班給付制度(加班前2小時,給予1.5倍加班費。)
(5)獎勵績效達成的旅遊活動
各營業單位可享有績效達成的績效獎金或國外旅遊活動全額獎勵。
(6)禮金發放
公司於員工婚喪喜慶時致贈禮金。
(7)膳食
工廠提供午餐供同仁食用,亦不定時增添下午茶以抒解員工壓力,增進工作效率。
2.進修及教育訓練:
本公司訂有教育訓練辦法,以透過組織系統實施為原則,對員工每年辦理GMP廠內部訓練;此外,為提升員工專業與產業競爭力,視需要不定期派員參加與工作業務相關之國內/外訓練課程或研討會。114年度員工參與外訓共計118人次,受訓總時數為813.95小時。
3.退休制度與其實施情形:
本公司訂有職工退休辦法,公司依法按月依精算報告提撥職工退休金,專戶儲存於台灣銀行,並依新修勞基法五十六條規定,足額提撥次年達到退休條件員工之退休金金額,114年度共有1位同仁榮退,另自九十四年七月一日起,本公司依「勞工退休金條例」規定,選擇或適用新制之同仁,公司依法按月依員工薪資6%提撥至勞工保險局之個人退休金專戶。
4.勞資間之協議情形與各項員工權益維護措施情形:
(1)本公司各項管理制度,係依勞基法及相關法令制訂及執行,並定期舉行勞資會議,協商員工權益維護措施,近來並增加留才誘因,如:公司庫藏股發放,員工認股權憑證及個人績效獎金的發放,在強調人性化、尊重個人的管理風格下,勞資關係和諧。
(2)為關懷弱勢族群,本司聘僱原住民及殘障人士為員工,力行符合政府宣導企業提供保障工作機會的理念。
(3)制定道德行為準則及工作場所性騷擾防治措施申訴及懲戒辦法等規則,維護員工權益。
(二) 列明最近年度及截至年報刊印日止,因勞資糾紛所遭受之損失(包括勞工檢查結果違反勞動基準法事項,應列明處分日期、處分字號、違反法規條文、違反法規內容、處分內容),並揭露目前及未來可能發生之估計金額與因應措施,如無法合理估計者,應說明其無法合理估計之事實:無。

| 日期 | 主旨說明 | 下載 |
|---|---|---|
| 2026.04.16 | 健亞/易威股份轉換案 健亞 新聞稿 | |
| 2026.04.16 | 健亞/易威股份轉換案 健亞投資人問答集 | |
| 2026.03.20 | 本公司與易威合併案--聲明稿 | |
| 2026.03.16 | 本公司與易威合併案--致股東信 | |
| 2026.03.12 | 本公司與易威合併案--新聞稿 | |
| 2025.05.06 | 健亞導入TrackWise Digital QMS與百昌攜手邁向品質管理與智能化新階段 | |
| 2024.11.29 | 113.11.29(五) 元富證券法人說明會資料。 法人說明會影音資料。 Click(外部連結) | |
| 2024.05.28 | Genovate Announces Plans to Submit a New Drug Application for PMR to the U.S. Food & Drug Administration in the Second Half of 2025。Click(外部連結) | |
| 2023.11.17 | 112.11.17(五) 元富證券法人說明會資料。 法人說明會影音資料。 Click(外部連結) | |
| 2023.11.15 | 本公司受邀參加元富證券112.11.17(五)舉辦之法人說明會,報名資訊請參閱附件。 | |
| 2022.10.20 | 元富證券法人說明會資料。 | |
| 2022.10.18 | 本公司受邀參加元富證券111.10.20(四)舉辦之線上法人說明會,報名資訊請參閱附件。 | |
| 2022.08.24 | 111.09.06(二) 健亞新竹地區徵才活動。 | |
| 2021.12.15 | C肝合併B肝療法研究登國際期刊,健亞利甘平合併C肝口服藥顯優勢。 Click(外部連結): | |
| 2021.11.19 | 本公司受邀參加元富證券舉辦之法人說明會。 | |
| 2020.09.11 | 國際聚焦超音波基金會(Focused Ultrasound Foundation)新聞發布介紹浩宇生醫NaviFUS系統在台灣進行之治療腦部膠質母細胞腫瘤(Glioblastoma)臨床試驗之報導。 ''New Clinical Trial for Focused Ultrasound in Glioblastoma'' Click(外部連結) | |
| 2020.09.09 | 生技產業趨勢與浩宇生醫的發展狀況 | |
| 2020.07.13 | 本公司受邀參加台新證券舉辦法人說明會 | |
| 2020.06.02 | 健亞羥氯奎進階版(GV17)提供安全選項 | |
| 2020.03.30 | 浩宇聚焦式超音波(NaviFUS )系統 ,衛福部核准與藥物併用臨床試驗 | |
| 2020.03.23 | 治療新冠肺炎,「老藥新用」HCQ成熱門話題 | |
| 2018.12.26 | 本公司受邀參加凱基證券舉辦法人說明會 | |
| 2018.11.21 | 有關本公司高血壓治療藥品 「壓穩膜衣錠80毫克」(衛署藥製字第056320號)與「壓穩膜衣錠160毫克」(衛署藥製字第056318號) 進行中之回收作業一案, 本公司發表聲明如附件: | |
| 2018.11.03 | 有關本公司高血壓治療藥品 「平壓妥膜衣錠」(衛部藥製字第058235號)進行中之回收作業一案, 本公司發表聲明如附件: | |
| 2018.03.29 | 本公司受邀參加證券櫃檯買賣中心舉辦之櫃買市場業績發表會,報告公司近況。 | |
| 2017.07.21 | 針對宇碩興業有限公司販售 「阿立批挫錠10毫克」(衛署藥製字第057320號,包裝規格為28’S/瓶裝)偽藥及進行中之回收作業一案, 本公司發表聲明如附件: |
進行中的開發項目以老年人疾病、改善生活品質等之治療劑為主,與一系列專利配方之改良長效劑型等。 並以結合政府資源及運用產業聯盟,切入新藥研發。
主要研發產品如下:
紅斑性狼瘡為自體免疫性疾病,全球患病率為每十萬人約3.2-517人,在亞洲好發於生育期婦女,台灣患病率為每十萬人37-98人,其中女性為每十萬人67-179人。發病時常因自體免疫系統攻擊,造成全身組織,例如皮膚、關節、血液、腎臟及神經系統的發炎。目前為止,疾病治療的五年存活期約90-95%,二十年存活期約78%,仍有相當大的進步空間。
羥氯喹寧(Hydroxychloroquine, HCQ)屬於抗瘧疾藥物,為紅斑性狼瘡的第一線用藥。其對於光敏性皮疹,如盤狀或亞急性狼瘡皮疹具有較好的療效,且能減少疾病的復發。
臨床數據顯示,長期使用HCQ的病患產生視網膜病變而導致失明的機率增加,一項回顧性分析顯示,持續使用HCQ超過五年的2361名病人中約有7.5%罹患視網膜病變,增加劑量與使用期間則比例增加。全身性紅斑狼瘡病患除了腎臟以外,心臟是其次受到免疫攻擊的器官,心血管疾病為SLE第三大死因。在SLE患者中,血管併發症的發生年齡比一般人年輕,一旦發生,死亡率約為一般人的兩倍。SLE較重度患者觀察到QTc延長,一項評估SLE疾病嚴重程度對QT離散度影響的研究發現,疾病活動度較高的患者QT離散度明顯更高。HCQ的使用不足以解釋血管併發症的增加,但是接受HCQ治療的患者的QT離散度往往更高。
GV17是HCQ右旋光學異構物,先前對於HCQ光學異構物各別的藥效、毒理及藥動狀態相關研究甚少。從健亞所完成的各項臨床前試驗顯示,GV17較HCQ藥效佳、安全性高且對於視網膜、腎臟及心臟的影響較小。關於GV17於治療紅斑性狼瘡以及預防心冠肺炎的用途已進行相關專利之申請,並已向美國FDA提出治療紅斑性狼瘡臨床試驗之Pre-IND諮詢,以規劃具體開發策略。同時與國內頂尖P3實驗室合作專題研究,測試其抗SARS-CoV-2病毒之活性,期許能成為優於HCQ之抗病毒藥物,早日進入臨床評估。
間歇性跛行是指步行一段距離後,患者會因下肢肌肉疼痛而無法繼續行走,但是在休息一會兒後,疼痛即自行消失。但當超過相同可預期的行走距離後,症狀會再度發生。間歇性跛行發生的主要原因是因為供給肌肉的血液和氧氣不足,而無法滿足周邊肌肉組織新陳代謝需求而導致。跛行發生的時間和部位直接與血管狹窄之程度與位置相關,屬於周邊動脈阻塞疾病的一種。
周邊動脈阻塞疾病是全身性動脈硬化的一種表現,它常與其他動脈粥狀硬化疾病如冠狀動脈疾病與腦血管疾病等有關。形成周邊動脈阻塞疾病的危險因子包括高血壓、高血糖、高血脂、高尿酸血症、抽煙等。周邊動脈阻塞疾病會導致下肢動脈血流減少,其症狀會隨病況嚴重程度而有所不同,最常見的是間歇性跛行、腿或足部有麻木感覺、嚴重時連不走路腳也會痛、甚至下肢潰瘍與傷口不易癒合等。周邊動脈疾病是中風、心肌梗塞等心血管疾病發作的重要警訊,患者需盡早接受適當治療,以降低心血管疾病發作之危險。
目前美國FDA核准使用於治療間歇性跛行有兩種藥物:(1)Pentoxifylline是1984年最先核准使用於治療間歇性跛行的藥物;之後,(2)1999年核准Cilostazol使用於治療間歇性跛行。Cilostazol為日本大塚製藥所開發,最早於1988年以商品名Pletaal在日本上市,台灣則於2000年核准上市。Cilostazol屬於可逆性PDE-3抑制劑,具有抗血小板凝集及血管擴張作用,此外,Cilostazol亦具有改善血脂(提升HDL和降低TG)的作用。
然Cilostazol的主要副作用─頭痛、心悸及腹瀉,常會造成患者停止服藥(近20%)。倘若能開發一長效緩釋且降低最高血中濃度之新劑型,將可滿足臨床上的需求。緣此,健亞是項新藥PMR已在台灣進行人體藥物動力學試驗與臨床二期療效試驗,結果顯示PMR符合目標藥物血中濃度曲線、療效及安全性,並已完成在美國提出新藥申請前須完成之樞紐性臨床試驗,藥物動力學統計分析報告顯示一天服用一次之PMR與一天服用兩次之美國核准對照藥品Cilostazol相較,其藥物血中濃度符合生體相等性之標準,達成主要療效指標。將依循美國FDA 5O5(b)(2)規定進行新藥查驗登記。
隨著現代人的生活型態改變,全球糖尿病人口遽增,糖尿病對於人類健康之威脅日益嚴重,已名列全球死亡原因的第四位;根據統計資料,預估到2025年將增加到3億人之多。而造成此健康問題主要是由於胰島素抵抗性或是胰島素分泌異常所導致的第二型糖尿病。關於糖尿病的治療,絕大多數的糖尿病患需要依賴口服降低血糖藥物,或是靠注射胰島素來控制血糖。然而上述之治療方式效果有限且耐受性不佳,同時還會伴隨明顯的副作用,因此迫切需要開發新型的治療方法或藥物。
DPP-IV抑制劑為治療第二型糖尿病之新型且有效的分子作用標的,於正常生理狀態下DPP-IV會快速分解代謝控制血糖平衡的分子GLP-1,因此GLP-1在人體血液中半衰期僅一分半鐘,目前GLP-1及其類似物Exenatide用於治療糖尿病時,必須以注射的方式給藥,十分不便,且伴隨的副作用如胃脹噁心不適等,造成病人對該類治療藥次接受度低。因此近年來發展DPP-IV抑制劑,以抑制DPP-IV活性進而增加GLP-1於血液中的濃度,藉以達到控制血糖之效果。
已知DPP-IV抑制劑對於治療糖尿病的優勢包括:
(1) 改善葡萄糖耐受度以及增加活體內胰島素分泌
(2) 敏銳地增加GIP以及GLP-1生物活性的累積程度
(3) 改善β細胞的葡萄糖反應
(4) 改善第二型糖尿病病人對於胰島素的敏感度
此類新藥中,首先開發成功者為美國藥廠Merck所發展之JanuviaTM (sitagliptin),於2006年底獲得美國FDA核准上市,可有效降低醣化血色素(HbA1c),臨床上常見的不良反應非常輕微,在治療上亦較少見體重增加和血糖過低的情況。根據報導,此藥物包含單複方產品,於2010年的銷售額高達33億美元。
由國衛院與健亞生技等產業聯盟團隊共同執行行政院科發基金之「促成生技成功投資案例」,已完成新穎抗糖尿病候選藥物DPP4抑制劑GBL121之臨床前試驗並成功完成在美國IND下的臨床一期試驗。大陸地區的開發與新藥登記,由合作夥伴石藥集團中奇製藥公司主導,已完成臨床二期試驗,目前進入臨床三期。
台灣約有300萬B型肝炎帶原病患,目前並無藥物可清除體內B型肝炎表面抗體,治療率不到5%。
利甘平膜衣錠(Livepro F.C. Tablets)為健亞已上市Entecavir(簡稱ETV)配方,用於治療有B型肝炎病毒複製跡象的成人慢性B型肝炎患者;TCM 800B為泰宗的冬蟲夏草菌絲體,其應用於肝硬化與非酒精性脂肪變性肝炎(non-alcoholic steatohepatitis, NASH)之治療已獲美國專利。本計畫將研究健亞ETV與泰宗TCM800B合併療法對B肝病毒表面抗原能陰轉的療效,提高治療率,且進一步降低或阻斷肝硬化。
計畫特色:
- 強力抑制肝臟中B型肝炎病毒的複製,減少肝臟細胞發炎。
- 強效降低病毒數量,副作用少,安全性佳。B肝控制率可達90%以上 。
- 低抗藥性,連續使用達5年,產生抗藥性的機率約1.2%。
該合併療法目前正於台灣進行臨床二期臨床試驗。
全身性紅斑狼瘡是一種自體免疫疾病,它可以侵犯身體的任何一個器官,而腎臟是其中最常受影響的器官之一;嚴重的狼瘡性腎炎如果不給予適當治療會進展到末期腎病,甚至死亡。
華人患者在初次診斷罹患紅斑性狼瘡後五年,併發腎臟疾病的盛行率為49%,其臨床表現包括蛋白尿、血尿、血清肌肝酸值上升、高血壓和尿毒症等;狼瘡性腎炎的華人患者,其五年與十年的腎臟存活率為74-84%,約有10%到15%的腎炎會進展至末期腎病。狼瘡性腎炎的早期發現且即時有效治療,有助於達到較高的疾病緩解率。
高劑量類固醇加上免疫抑制劑或細胞毒殺藥物(cytotoxic agent)是現今治療該疾病的主流。近年來,原用於抗排斥的免疫抑制劑Mycophenolate mofetil(簡稱MMF),用於增生性狼瘡腎炎的誘導治療或維持治療都有很好的效果。2012年美國風濕病學會治療指引建議狼瘡性腎炎之維持性治療:(1)MMF每天1~2g或(2)Azathioprine(簡稱AZA)每天每公斤體重2mg,並視情況搭配低劑量類固醇。臨床使用上,MMF漸躍居為狼瘡性腎炎維持性治療之第一線標準用藥,乃基於其療效優於AZA,包括延後治療失敗發生時間以及出現較少嚴重不良事件等。一項以台灣患者的研究顯示,MMF低劑量(每天0.5-1公克)與糖化皮脂類固醇(glucocorticoids)併用為一安全且具成本效益的狼瘡性腎炎療法。
MMF用於狼瘡性腎炎的治療費用,在部分亞洲國家,包括韓國、馬來西亞以及中國大陸等,已有全民醫療保險給付,但在台灣尚未納入給付項目。
依據中華民國風濕病醫學會之陳情與衛生福利部食品藥物管理署之建議下,我們相信為本公司已上市MMF配方喜妥善膠囊(Mycocep capsules)爭取此新適應症之核准,以滿足台灣SLE患者的醫療需求並減輕其經濟負擔,是我們的任務。本藥品目前已完成臨床試驗與新適應症之查驗登記,提供台灣SLE患者多一種用藥選擇。
健亞於民國84年增資前之創業期間為一新藥研發中心,主要工作為協助母公司,美國健亞科技公司(Genelabs Technologies, Inc.),找尋抗病毒、抗癌新藥、以及在抗肝癌新藥研究上建立篩選方法。增資後積極投入各項藥品的臨床試驗,另外也進行劑型研發,開發緩釋劑型藥物。
研發成果詳列如下:
紅斑性狼瘡(Lupus)是一種自體免疫系統病變所引起的長期終身疾病,目前並無妥善的治療方式。除會影響皮膚、肌肉、關節外,可導致其它器官如心、肺、腎、神經,以及造血器官的慢性發炎。但多數患者,都有高潮與低潮或緩解的交替病程,有的甚至長期完全沒有病狀的緩解,並且不能治癒。GL701的活性成份DHEA (dehydro-epiandrosterone)乃人體自然可產生的雄性荷爾蒙。一般說來,紅斑性狼瘡病人體內的DHEA濃度較正常人為低。
在史丹褔大學進行的研究顯示,輕度和中度紅斑性狼瘡病人服用DHEA後,可安全和有效地控制疾病。健亞與美國Genelabs(GLT)同步,在台灣四大醫院免疫風溼科,同時進行第三期臨床試驗。健亞在台灣完成的臨床試驗數據,與GLT 在美國的臨床數據合併,在2000/9完成向美國食品藥物管理局(FDA)申請新藥核准的送件程序。雖然2001/6收到未核准信函(non-approvable letter),但之後積極與FDA溝通以謀解決之道,並依照FDA建議,於2002/2完成補充臨床及分析資料呈送。這些資料顯示GL701施用於全身性紅斑狼瘡之女性病患,於併用低劑量的類皮質糖(glucocorticoids)的情況下,可改善骨質密度之流失。
GLT於2002/8/28接獲FDA核發新藥申請可批准函(Approvable letter)。健亞繼續與GLT同步於台灣六大醫學中心展開有關骨質密度的臨床試驗,雖然結果仍未能達到療效上的明顯統計意義,但延長治療至18個月時,可達到維持骨質密度的主要療效。2007/4 Genelabs與FDA就未來NDA核准所進行的SPA (Special Protocol Assessment)達成協議,Genelabs可藉此設計新的臨床試驗以完成新藥開發。
GL701是有史以來第一次由國人執行的世界性新藥開發工作,除了代表國內生技製藥的里程碑外,健亞亦是台灣第一家與GLT共同向美國FDA與台灣衛生署提出NDA者。在超過八年的研發過程中,藉由Genelabs的協助下,早在1996年,國內藥廠才剛開始從事單一中心供查驗登記之臨床試驗時,健亞就已開始進行大規模的多中心新藥Phase III臨床試驗,並藉此建立了完整的臨床試驗團隊。對提昇國內臨床試驗水準,貢獻卓著。開發GL701的過程中,在台灣,研發新藥從遙不可及的夢想,逐漸成為可計算風險的計劃,健亞參與本計劃的研發工作,深覺與有榮焉。
開發過程
里程碑
1992~1993 Genelabs與Stanford大學合作,完成Phase I/II臨床試驗
1994~1995 Genelabs在美國進行192 SLE病人Phase III臨床試驗
1995/11 Genelabs技轉成為增資後GBL三大新藥計畫之一
1997/3~1999/7在三總、長庚、北榮、中榮進行120 SLE (全身性紅斑狼瘡)病人Phase III臨床試驗
1997/3 “GL701對全身性紅斑狼瘡患者的第三期臨床試驗” 獲科學園區創新計畫核准,補助款250萬元,執行期間1997/1~1999/12.
2000/5~2000/9 Genelabs合併381人及健亞120人Phase III臨床試驗結果,送交美國食品藥物管理局(FDA)審查。
2001/6接獲FDA未核准信函(non-approvable letter)
2002/3獲頒衛生署90年度藥物科技研究發展獎藥品類銅牌獎 “抗紅斑性狼瘡新藥思樂依”
2002/2 Genelabs完成骨質密度臨床分析補件
2002/8接獲FDA新藥申請可批准函(approvable letter)
2003/1~2004/8 Genelabs在美國進行150位SLE病人骨質密度變化之Phase III臨床試驗(療程6個月)
2004/10 Genelabs宣佈初步臨床試驗結果,未達到主要療效。
2003/9~2005/2在北榮、台大、馬偕、長庚、中榮、彰基進行80位SLE病人骨質密度變化之Phase III臨床試驗(療程9個月)
2005/4 Genelabs宣佈健亞執行的80位SLE病人骨質密度變化之Phase III臨床試驗,未達療效上明顯的統計意義。
2005/8 Genelabs宣佈前次臨床試驗,延續治療期至18個月,可達到維持骨質密度的主要療效。
2007/4 Genelabs與FDA就其未來NDA所需進行SLE Phase III之SPA (Special Protocol Assessment)達成協議。
2008/11 GSK購併Genelabs, 本計劃隨之終止。
GL331為Genelabs, University of North Carolina及美國國家癌症研究所(National Cancer Institute)共同開發的新抗癌藥物。GL331的化學結構雖與現今使用最多的抗癌藥物之一的Etoposide類似,但在試管試驗中顯示它能克服抗藥性(Multiple Drug Resistance)。抗藥性為造成癌症治療與控制上一個嚴重的問題。Genelabs於1993/4在德州休斯頓的M.D. Anderson Cancer Center進行臨床第I期人體試驗。第I期臨床實驗本在尋找GL331的最大安全劑量,可是在部份病人中已發現療效。
健亞除在合成GL331的衍生物上有所貢獻外,與國家衛生研究院合作,在榮總已完成對胃癌病患作第I/II期臨床試驗,結果發現安全性良好。GL331是首度由國人在台灣執行的第I/II期臨床試驗,對提升台灣臨床試驗水準具有很大的貢獻。因為已失去市場時效性,GL331新藥開發計劃於1999年中止。
紫杉醇(paclitaxel)主治乳癌、卵巢癌、非小細胞肺癌(non-small cell lung cancer)。健亞在工業局主導性新產品計畫的補助下於民國1998/6/30完成原料藥開發。可將紫杉醇的純度由10%提高至>98.5%。同時健亞開發的紫杉醇針劑新配方─欣沛方(Genetaxyl),與原市售品紫杉醇學名藥,最大差異在於大幅度降低 Cremophor和乙醇的用量,增加紫杉醇的穩定性和溶解,並進而降低Cremophor造成的毒 性,減少病人使用紫杉醇針劑產品的副作用。此新處方已由經濟部智慧財產局核准專利。
GenetaxylTM (欣沛方)所進行的各項研究開發,如下:
(1) 原料藥的開發
(2) 藥物動力學試驗
(3) 乳癌臨床試驗
(4) 鼻咽癌及非小細胞肺癌臨床試驗
(5) 食道癌臨床試驗
(6) 口服Genetaxyl臨床試驗
其中在台北榮總與馬偕執行的Phase II乳癌臨床試驗(29人),臨床結果已當作申請藥證的送件資料,並於92/1/21獲衛生署核准藥證。
開發過程
里程碑
1993~1995 Genelabs開發新組成劑型
1995/11 Genelabs技轉成為增資後GBL三大新藥計畫之一
1996~1997分別在生技中心與美國SRI進行動物毒性試驗,證實Genetaxyl安全性優於Taxol.
1996/12 “紫杉醇原料藥之開發” 獲工業局主導性計畫核准,補助款370萬元,執行期間1996/7~1999/12.
1998/6~2000/1在北榮和長庚進行Phase I臨床試驗
1998/6 “紫杉醇針劑─健泰速開發計畫” 獲工業局主導性計畫核准,補助款1141萬元,執行期間1998/10~2003/9.
1999/6衛生署核准紫杉醇”健亞” 原料藥藥證
1999在明生進行藥物動力學試驗
2000/9~2002/5在北榮和馬偕進行供查驗登記之29人乳癌Phase II臨床試驗
2000/12~2002/7在和信進行10人NPC(鼻咽癌)臨床試驗研究
2001/6~2003/7在和信進行28人NSCLC(非小細胞肺癌)臨床試驗研究
2002/1 “紫杉烷類組成物” 獲准中華民國專利,專利期間2002/1~2014/3
2003/1衛生署核准 ”欣沛方注射劑” 藥證
2003/8獲頒衛生署91年度藥物科技研究發展獎藥品類銀牌獎 “紫杉醇針劑欣沛方”
2003/8~2005/10在長庚進行13人食道癌臨床試驗研究
2003/9 “抗癌藥物Genetaxyl用於復發性食道癌之Phase II之臨床試驗” 獲科學園區創新計畫核准,補助款150萬元,執行期間2003/9~2005/8.
2003/11健保局核准“欣沛方注射劑” 給付藥價
2003/12~2005/5在北榮和長庚進行21人口服Genetaxyl臨床試驗
2004/3 “口服紫杉醇抗癌藥Genetaxyl先期研究計畫” 獲經濟部SBIR計畫核准,補助款75萬元,執行期間2004/4~2004/9
輕鬆免除大腸鏡前的清腸恐懼
「健亞」與「景安」攜手成功開發新一代清腸劑
隨著工商腳步快速,國人飲食西化,愛吃油炸、燒烤與加工肉品等食物,造成大腸癌患者增加。依據國民健康署公佈之最新統計,2012年台灣地區癌症排行榜,大腸癌第7度奪冠;比前一年罹患人數增加14,965人,平均每35分6秒就新增一名大腸癌患者。國健署分析,因著大腸癌案例激增,民眾的警覺心增加,導致健檢意識抬頭,許多人願意接受大腸癌篩檢,當年就增加了33萬名篩檢民眾。
大腸癌的篩檢中,大腸鏡檢查是最確實及可靠的方法,因為「無痛」的普及,許多人不會對受檢過程中侵入性的不適感而害怕,反而是受不了檢查前的清腸過程,心生畏懼。第一代的清腸劑需服用大量藥液(2,000~4,000 c.c.),受檢者往往無法順利完成清腸。第二代清腸劑,藥液服用量大幅度降低(每次僅數十毫升),唯屬鹽類清腸劑,鹹澀之口感也有部分受檢者較難接受。
第三代清腸劑-Bowklean powder(保可淨散劑)以類似505b2新藥模式,由景安委託健亞於2012年7月開始切入劑型研究,進入開發流程,突破專利障礙及困難的製程設計;景安更斥資執行600人之大型臨床療效試驗,以腸道清潔程度為指標,試驗結果證實Bowklean優於對照組(Klean-Prep),能夠徹底清腸,產生較少泡沫,提高檢查之準確性。整個開發時程歷時3年半,於日前取得藥證。
業界知名專業醫藥行銷公司-景安興業邱謝俊董事長表示:Bowklean服用時調製之藥液量較少,並有檸檬香甜味,可免除市面上其他產品需喝大量藥液引起腹漲、噁心、嘔吐之缺點。此外,BowKlean的藥效反應較為溫和,可緩和腹瀉時的腹絞痛,在使用上「親民」許多,對大腸鏡的受檢者來說是一大福音。
Bowklean的開發亦落實健亞一路走來「研發新藥,體貼國人健康」的企業使命。此外,健亞除了是生產製造廠外,亦擁有台灣以外之市場開發權,健亞將於適當的市場評估後,選擇進一步開發海外市場,進行查驗登記之申請,後勢可期。
Bowklean powder與其他市售品之比較:
清腸劑三代
(Bowklean Powder)
清腸劑二代
(F 產品)
清腸劑一代
(K 產品)
服用量
***
(量少 150ml)
**
(量少 300ml)
*
(量大 2,000ml)
口感
***
(檸檬清香易入口)
*
(鹹,需以飲料調製)
*
(口感不佳,具化學味)
腸道氣泡量#
***
(氣泡少)
*
(有大顆氣泡)
*
(有綿細氣泡)
清腸作用
作用溫和。
作用急速。
作用緩慢,需搭配瀉藥。
副作用
鮮少副作用。
噁心、嘔吐、 電解質失衡。
腹賬、噁心、 嘔吐。
註 # :泡泡容易影響腸鏡的觀察。
現階段已完成具生體相等性(BE)劑型開發產品計有:Lisinopril, Doxazosin, Loratadine, Alprazolam, Hydroxychloroquine, Zopiclone, Mephenoxalone, Alprazolam SR, Felodipine SR, Galanthamine, Nateglinide, Desloratadine, Atorvastatin, Clopidogrel, Montelukast, Mycophenolate mofetil, Valsartan, Rosuvastatin, Aripiprazole, Entecavir, Irbesartan 。這些產品大多是在尚無國產藥品出現時開始研發,並居於學名藥市場銷售領先地位。
緩釋劑型的技術已成功的使用在一些治療性藥劑上。健亞自行研發的第一個產品Alprazolam 緩釋劑型(健得靜持續性藥效錠)已完成生體相等性試驗並於2001年上市,成為國資廠研發的第一品牌。而呼吸道疾病治療劑(ASR, 樂咳痰舒長效錠),以及與美國Oregon University合作開發的糖尿病緩釋劑型(GSR, 糖舒平長效錠)也已完成臨床試驗,分別於2005和2006年上市。
GSR開發過程
里程碑
1997/2與美國Oregon州立大學簽約委託開發劑型
1999/6 Oregon大學技轉健亞
2000/11~2001/4在長庚進行第一次BA臨床試驗
2001/1~2002/10在長庚進行40人藥效臨床試驗
2002/3~2002/8在長庚進行第二次BA臨床試驗
2002/2 “緩釋降血糖藥物GSR之BA臨床試驗” 獲科學園區創新計畫核准,補助款150萬元,執行期間2001/12~2002/11.
2002/12完成BA和藥效臨床試驗報告
2005/2衛生署核准“糖舒平長效錠” 藥證
除GSR, ASR之外,急迫性尿失禁用藥”優合”(PPV)已於2002/7完成臨床試驗資料的送件,並在2003/11取得藥證。2004年初上市。
在七七公告時期(1993/7~2000/12),衛生署已建立了新藥查驗登記須在國內進行臨床試驗的準則,印度的原料藥廠未如今日般快速有效地開發各種原料藥,而醫藥業的全球化尚未全盤展開之際,將在其他少數國家暢銷的藥品,設法合成少量原料藥,並在台灣執行40人查驗登記用的臨床試驗,以取得藥證上市,成為有利可圖的開發產品型態:區域新藥。
PPV正是一種區域新藥。它在1999年以前只在德、法、英、日、韓上市,是一種溫和有效的尿失禁治療藥。健亞擁有自己的臨床試驗與原料藥開發團隊,因此是國內最適合開發這一類新藥的公司。開發的過程大致順利,短短四年內,完成了原料藥開發、藥物的動物毒性試驗、BA與藥效的臨床試驗、以及藥品查驗登記,同時也申請了政府計劃,充分顯示健亞多才多藝的特性。
PPV開發過程
里程碑
1999進行動物毒性試驗
2000~2001原料藥製程開發
2000/11~2002/5在中醫、北醫、長庚進行40人藥效臨床試驗
2000/12 “急迫性尿失禁用藥─優合產品開發計畫” 獲工業局主導性計畫核准,補助款717萬元,執行期間2000/4~2002/9.
2001/11~2002/1在佳生進行BA臨床試驗
2003/6衛生署核准“鹽酸普比威林” 原料藥藥證
2003/8衛生署核准“優合膜衣錠” 藥證
LNC是一種新型的降血脂藥物,包含一個Niacin為主成份的緩釋核心(NSR),以及核心表層含有Lovastatin之塗層。緩釋核心(NSR)須控制Niacin的釋放速度,使得與外層難溶之Lovastatin達到藥效的協同,並且須避免較大的藥體崩解而快速溶出大量Niacin。此外,Lovastatin藥量僅有Niacin之4%,如何控制每錠之間塗層藥量之均勻度,具有技術上的挑戰。
LNC與NSR原先是以獨立的產品各自開發。依照七七公告的法規,進行40人臨床藥效試驗以及BA試驗。由於Niacin在國內從未用於降血脂,並因劑量較大具有若干安全上的疑慮,因此藥政單位對於BA試驗的設計與結果,採取較為嚴格的方式審查。於是NSR的審查結果也影響了LNC的查驗登記。經與藥政單位不斷溝通,最後協議進行NSR第二次BA試驗,當作NSR與LNC兩者核准的條件。
LNC與NSR的漫長開發過程,充份顯示健亞對於開發藥物,在技術面與法規面,克服各種困難的堅忍與決心。
LNC開發過程
NSR開發過程
里程碑
2003/9~2005/6在馬偕、北榮、三總、振興進行40人藥效臨床試驗
2003/10~2005/8在長庚、中榮、三總進行40人藥效臨床試驗
2006/6 LNC臨床試驗報告備查
2006/8 NSR臨床試驗報告備查
2004/3~2004/6第一次BA試驗
2004/3~2004/7第一次BA試驗
2007/7 LNC BA報告備查
(等候NSR BA試驗結果)
2009/3~2009/6第二次BA試驗
2010/2 NSR BA報告備查
2010/10衛生署核准NSR藥證
(優脂持續釋放錠)
2011/5重新查驗登記送件
2012/5衛生署核准LNC藥證
(理脂膜衣錠)
降尿酸/痛風新藥
AZ於2012年4月以13億美元收購 Ardea Biosciences。主要原因是因爲 lesinurad/RDEA594(URATI inhibitor)臨床Ⅱ期結果不錯。Lesinurad已於12/22/2015獲得美國FDA批准。
食研所於2012年成功的篩選出可食用的潛力菌株, 一組對 XO inhibition有活性(動物與酵素實驗),一組對分解尿酸有活性的潛力菌株。經過發酵條件最適化與相關活性物質(Biomarker)探索取得初步成功後 ,目前已正式進入量產商業化階段。
微生物降尿酸(乳酸菌、納豆菌、麴菌、 醋酸菌)專利搜尋發現近5家日本廠商(Meiji, Sanwa Shurui Co., …etc.)也在進行類似研發,明治於2015年3月上市兩種Yogurt , 訴求控制尿酸。
台灣尿酸過高(超過 7mg/dL)的患者超過200萬人。特別是30歲至55歲以上中年男性,罹患高尿酸血症的比例更達25%。如何開發一 “User Friendly”的產品(不論預防或治療), 有迫切的需求。
健亞正與食研所、泰宗、金穎合作,藉由A+計畫補助,除了希望早日能上市「食品」,嘉惠病患外 ,也規劃以研發「健」字號產品或「化療漾」開發模式的中藥新藥 ,同時已展開對 Biomarker 中的活性物質進行藥物開發,創造「台灣優先, 世界第一」的新藥潛力商機 。
a) 民國88年獲頒“科學工業園區研究發展投入獎”
b) 榮獲衛生署“九十年度藥物科技研究發展獎”藥品類銅牌獎 (抗紅斑性狼瘡新藥“思樂依”)
c) 榮獲衛生署“九十一年度藥物科技研究發展獎”藥品類銀牌獎 (紫杉醇針劑“欣沛方”)
d) 榮獲衛生署“九十五年度藥物科技研究發展獎”藥品類銅牌獎 (降血糖緩釋藥物“糖舒平長效錠”)
e) 榮獲衛生署“九十五年度藥物科技研究發展獎”藥品類銅牌獎 (急迫性尿失禁藥物“優合” 與原料藥“鹽酸普比威林”)
a) “紫杉烷類組成物”,中華民國專利公告號471972,申請日 1996/03/12,公告日2002/01/11,權止日014/03/11。
b) “MODULATION OF INTERLEUKIN-10 BY DHEA” 美國專利 申請日2003/07/18,2005/01/20公開。
c) “鹽酸普比威林的製備方法”,中華民國專利申請案號092131618, 申請日2003/11/12,2005/05/16公開。
d) “取代之2-苯基塞二唑和2-苯基噁二唑化合物,及其作為黃嘌呤氧 化酵素抑制劑之用途”,中華民國專利申請案號095120598, 申請日2006/06/09。
e) “抗嘔吐貼片”,中華民國專利申請案號098136765,申請日 2009/10/29,2010/10/28公開。
f) “經控制釋放的水凝膠配方”,中華民國專利公告號 I400096,申 請日2007/09/04,公告日2013/07/01,權止日2027/09/03。
曾獲得政府相關計畫輔導或補助
金額單位:千元
政府相關計畫名稱:科學園區創新技術研究發展計畫
申請計畫名稱:抗肝癌藥劑之發現發展及研究
執行期間: 83年1月~83年12月
計畫主持人:Paul Chow
計畫投入人力: 21人月
研發重點:合成Podophyllotoxins, 2-phenyl-4-quinolones類化合物共33種,其中8種化合物抑制人類肝癌細胞株生長優於已上市抗癌藥VP-16, VM-26, doxorubicin。化合物25和GL2228初步證實具有良好細胞毒性選擇性和抗抗藥性,並可提高植有血癌或大腸癌細胞老鼠的存活天數。
計畫總經費
政府補助款
自籌款
3,590
1,500
2,090
金額單位:千元
政府相關計畫名稱:工業局主導性新產品開發計畫
申請計畫名稱:紫杉醇原料藥之開發
執行期間: 85年7月~87年6月
計畫主持人:陳正
計畫投入人力: 96人月
研發重點:開發一項流程,將純度約10%之紫杉醇,經過三步驟純化,提高純度至合乎醫藥品級之>98.5%。此流程適用於公斤級原料藥生產。
計畫總經費
政府補助款
自籌款
15,068
3,700
7,668
金額單位:千元
政府相關計畫名稱:科學園區創新技術研究發展計畫
申請計畫名稱:GL701對全身性紅斑性狼瘡患者的第三期臨床試驗
執行期間: 86年1月~89年9月
計畫主持人:劉致顯
計畫投入人力: 47人月
研發重點:完成在三總、長庚、北榮、中榮進行120 SLE (全身性紅斑狼瘡)病人Phase III臨床試驗。
計畫總經費
政府補助款
自籌款
8,388
3,900
4,488
金額單位:千元
政府相關計畫名稱:工業局主導性新產品開發計畫
申請計畫名稱:紫杉醇針劑─健速泰產品開發計畫
執行期間: 87年10月~92年9月
計畫主持人:陳正
計畫投入人力: 270人月
研發重點:以改良劑型的紫杉醇針劑Genetaxyl在台北榮總與馬偕醫院進行Phase II乳癌臨床試驗(29人),另外在和信醫院進行Phase II 頭頸癌與非小細胞肺癌臨床試驗。乳癌的臨床結果已作為申請藥證的送件資料,並於92/1取得藥證。
計畫總經費
政府補助款
自籌款
47,600
11,420
24,760
金額單位:千元
政府相關計畫名稱:工業局主導性新產品開發計畫
申請計畫名稱:急迫性尿失禁用藥─優合
執行期間: 89年4月~91年9月
計畫主持人:張啟泰
計畫投入人力: 226人月
研發重點:(1) 改良製程、開發原料藥Propiverine HCl.(2) 在林口長庚醫院進行40人的藥效試驗,臨床試驗的結果已於91/7向衛生署提出報告,並於92/11取得藥證。
計畫總經費
政府補助款
自籌款
39,480
7,170
25,140
金額單位:千元
政府相關計畫名稱:科學園區創新技術研究發展計畫
申請計畫名稱:緩釋降血糖藥物GSR之BA臨床試驗
執行期間: 90年12月~91年11月
計畫主持人:陳正
計畫投入人力: 29人月
研發重點:以長效型的GSR與短效型的Glipizide藥物作對照,完成在林口長庚醫院進行的24人生體可用率試驗。試驗目的為評估兩種藥物在非胰島素依賴型糖尿病病患之生體可用率。
計畫總經費
政府補助款
自籌款
3,570
1,700
1,870
金額單位:千元
政府相關計畫名稱:科學園區創新技術研究發展計畫
申請計畫名稱:抗癌藥物Genetaxyl用於復發性食道癌之Phase II臨床試驗
執行期間: 92年9月~94年8月
計畫主持人:陳正
計畫投入人力: 50人月
研發重點:以改良劑型的紫杉醇針劑Genetaxyl在林口長庚醫院進行復發性食道癌的Phase II臨床試驗。本計畫以完成前13位病人療效與安全性的初步評估為目標。
計畫總經費
政府補助款
自籌款
4,757
1,800
2,957
金額單位:千元
政府相關計畫名稱:技術處鼓勵中小企業開發新技術推動計畫
申請計畫名稱:口服紫杉醇抗癌藥Genetaxyl先期研究計畫
執行期間: 93年4月~93年9月
計畫主持人:朱紫汀
計畫投入人力: 20人月
研發重點:紫杉醇抗癌藥Genetaxyl與環孢靈(cyclosporine A)以口服的方式合併使用,在林口長庚醫院進行21人的臨床試驗。本計畫分析受試者血中藥物濃度,以說明口服Genetaxyl之藥物動力學性質。
計畫總經費
政府補助款
自籌款
2,608
750
1,858
金額單位:千元
政府相關計畫名稱:技術處鼓勵中小企業開發新技術推動計畫
申請計畫名稱:痛風新藥開發先期研究計畫
執行期間: 94年7月~95年3月
計畫主持人:陳正
計畫投入人力: 22.5人月
研發重點:以痛風新藥Febuxostat為改良目標,合成一系列分子空間配置類似,核心雜環不同的類似物。期望在有限的合成目標中,找到藥效活性接近Febuxostat的分子。這分子本身,或者包含再進一步結構修飾後,可成為後續動物試驗與人體臨床試驗開發的基礎。
計畫總經費
政府補助款
自籌款
9,000
3,000
6,000
金額單位:千元
政府相關計畫名稱:技術處鼓勵中小企業開發新技術推動計畫
申請計畫名稱:痛風新藥開發計劃
執行期間: 96年6月~98年5月
計畫主持人:陳正
計畫投入人力: 25.1人月
研發重點:先期研究階段獲得的先選藥(Lead),經結構修飾後,進行初步的動物試驗,包含藥效、藥物動力學和毒理試驗,以期找出候選藥(Candidate)
計畫總經費
政府補助款
自籌款
15,000
5,000
10,000
金額單位:千元
政府相關計畫名稱:經濟部業界開發產業技術計畫─快速審查臨床試驗計畫
(Fast Track)
申請計畫名稱:PMR藥物動力學試驗計劃
執行期間: 98年6月~98年11月
計畫主持人:陳金平
計畫投入人力: 3.6人月
研發重點:進行PMR與Pletaal錠劑由男性健康受試者在禁食情況下口服的藥物動力學試驗,包括12人的單劑量試驗與6人的多劑量試驗。
計畫總經費
政府補助款
自籌款
1,700
714
986
金額單位:千元
政府相關計畫名稱:經濟部業界開發產業技術計畫─快速審查臨床試驗計畫
(Fast Track)
申請計畫名稱:GranPatch藥物動力學試驗計劃
執行期間: 99年5月~99年8月
計畫主持人:陳啟祥
計畫投入人力: 3.6人月
研發重點:進行止吐貼片GranPatch單劑量平行之藥物動力學試驗,包括至少男性與女性各12人,評估Granisetron之吸收速度與吸收程度。
計畫總經費
政府補助款
自籌款
2,600
1,040
1,560
藥事法規定,非藥商不得為藥物廣告。
本公司網站產品資訊均為許可證持有者,且刊載內容即為主管機關核准之仿單內容。
訪客若非醫療專業人員,應尋求醫師之診斷與指示,不宜僅依仿單資訊自行判斷以免耽誤病情
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
失智藥 |
欣憶膜衣錠8毫克 |
衛署藥製 |
047265 |
治療Alzheimer症輕度至中度嚴重痴呆 |
安眠藥 |
米達諾注射劑5公絲/5公撮 |
衛署藥製 |
044436 |
知覺鎮靜、急救加護病房鎮靜、麻醉誘導及維持、手術前給藥 |
米達諾注射劑5公絲/公撮 |
衛署藥製 |
044437 |
知覺鎮靜、急救加護病房鎮靜、麻醉誘導及維持、手術前給藥 |
|
健康得眠膜衣錠7.5公絲 |
衛署藥製 |
043460 |
失眠症 |
|
抗思覺失調症藥 |
"健亞"阿立批挫錠10毫克 |
衛署藥製 |
057320 |
成人和青少年 (13至17歲)的思覺失調症。 |
"健亞"阿立批挫錠15毫克 |
衛署藥製 |
057364 |
成人和青少年 (13至17歲)的思覺失調症。 |
|
抗焦慮劑 |
"健亞"健得靜錠0.25公絲(三氮二氮平) |
衛署藥製 |
042948 |
焦慮狀態、恐慌症 |
"健亞"健得靜錠0.5公絲(三氮二氮平) |
衛署藥製 |
042514 |
焦慮狀態 |
|
健得靜持續性藥效錠1.0公絲 |
衛署藥製 |
044011 |
焦慮狀態、恐慌症 |
|
抗癲癇劑 |
癲合膜衣錠300毫克 |
衛署藥製 |
047689 |
成人局部癲癇發作之單一或輔助治療,大於一個月孩童癲癇局部發作之輔助治療 |
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
休克治療劑 |
健多博注射液12.5毫克/毫升(多保他命) |
衛署藥製 |
042141 |
增強心肌收縮力而適用於短期治療器質性心臟病、心臟外科手術引起心肌收縮力抑制而導致之心臟代償機能衰竭 |
抗血小板凝集劑 |
栓暢膜衣錠75毫克 |
衛署藥製 |
049967 |
*降低近期發生中風、心肌梗塞或周邊動脈血管疾病的粥狀動脈硬化病人之粥狀動脈栓塞事件(如:心肌梗塞、中風或其他因血管病變引起的死亡)*與aspirin 併用降低非ST 段上升之急性冠心症(不穩定性心絞痛和非Q 波型心肌梗塞)病人(包括經皮冠狀動脈介入性治療後放置支架的患者)之粥狀動脈栓塞事件。*與aspirin 併用可用於以內科治療的ST 段上升之急性心肌梗塞病人。 |
降血脂劑 |
洛脂平膜衣錠10毫克 |
衛署藥製 |
057130 |
高膽固醇血症、高三酸甘油酯血症 |
降脂妥膜衣錠10毫克 |
衛署藥製 |
049543 |
高膽固醇血症、高三酸甘油脂血症。對於臨床上沒有冠心病的第二型糖尿病患者,但是至少有任一其他冠心病危險因子,包括高血壓、視網膜病變、白蛋白尿、或吸菸,Atorvastatin適用於:降低心肌梗塞的風險、降低中風的風險。降低冠心病高危險群的心血管事件發生率. 對於臨床上沒有冠心病的高血壓患者,但是至少有三個其他冠心病危險因子,包括第二型糖尿病、年紀大於等於55歲、微白蛋白尿或蛋白尿、吸煙或第一等親在55歲(男性)或60歲(女性)曾發生冠心病,Atorvastatin適用於:降低心肌梗塞的風險、降低中風的風險、降低血管再造術與心絞痛的風險。 |
|
降脂妥膜衣錠20毫克 |
衛署藥製 |
052530 |
高膽固醇血症、高三酸甘油脂血症。對於臨床上沒有冠心病的第二型糖尿病患者,但是至少有任一其他冠心病危險因子,包括高血壓、視網膜病變、白蛋白尿、或吸菸,Atorvastatin適用於:降低心肌梗塞的風險、降低中風的風險。降低冠心病高危險群的心血管事件發生率. 對於臨床上沒有冠心病的高血壓患者,但是至少有三個其他冠心病危險因子,包括第二型糖尿病、年紀大於等於55歲、微白蛋白尿或蛋白尿、吸煙或第一等親在55歲(男性)或60歲(女性)曾發生冠心病,Atorvastatin適用於:降低心肌梗塞的風險、降低中風的風險、降低血管再造術與心絞痛的風險。 |
|
降血壓劑 |
平壓妥膜衣錠300毫克 |
衛部藥製 |
058235 |
本態性高血壓。治療併有高血壓及第二型糖尿病患者的高血壓及糖尿病性腎病變 |
健諾心錠2公絲(甲磺酸多薩坐辛) |
衛署藥製 |
042378 |
高血壓、良性前列腺肥大 |
|
健諾心錠4公絲(甲磺酸多薩坐辛) |
衛署藥製 |
042874 |
高血壓、良性前列腺肥大 |
|
狹心症治療劑 |
怡心通注射液0.1% |
衛署藥製 |
044974 |
治療狹心症之發作 |
您可諾錠5毫克 |
衛署藥製 |
049306 |
狹心症 |
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
紅斑狼瘡,關節炎治療劑 |
"健亞"殲瘧膜衣錠200毫克(硫酸羥氯奎寧) |
衛署藥製 |
042899 |
1.圓盤狀及全身性紅斑性狼瘡2.慢性多形日光疹3.慢性風濕性關節炎4.鏈狀瘧原蟲和間日瘧原蟲引起之瘧疾。 |
消炎止痛藥 |
艾希克膜衣錠100毫克 |
衛部藥製 |
058604 |
治療退化性關節炎、類風溼性關節炎、僵直性脊椎炎所引起之疼痛及發炎症狀 |
骨骼肌鬆弛劑 |
"健亞"健樂舒錠200公絲(每非歐隆) |
衛署藥製 |
042743 |
緩解由脊髓或肌肉痙攣引起的疼痛 |
卡力舒錠250毫克 |
衛署藥製 |
055961 |
焦慮緊張症,經常緊張,肌炎,椎間神經痛,坐骨神經痛,頸痛,風濕性關節炎,骨關節炎,肌肉僵硬,肌肉痛。 |
|
"健亞"健舒注射液10毫克/毫升(艾翠克瑞) |
衛署藥製 |
042879 |
本藥乃一高選擇性及競爭性的非去極化神經肌肉阻斷劑。可作為手術全身麻醉或加護病房鎮靜的輔助劑、以鬆弛骨骼肌、幫助氣管插管與人工吸器的協調。 |
|
若可麻注射劑10毫克/毫升 |
衛部藥製 |
058097 |
全身麻醉的輔佐藥,以幫助支氣管內插管、提供手術需快速麻醉誘導時骨骼肌肉鬆弛狀態、加護病房中需插管及使用人工呼吸器時 |
|
妥適膜衣錠50毫克 |
衛署藥製 |
056735 |
反覆發生的疼痛性肌痙攣及腦部血管病變所導致之肌張力異常升高 |
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
免疫抑制劑 |
喜妥善膠囊250毫克 |
衛署藥製 |
050866 |
與 Cyclosporin 和類固醇合併使用,以預防或緩解腎臟移植之急性器官排斥、預防心臟和肝臟移植之急性器官排斥。 |
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
抗黴菌劑 |
健那諾靜脈注射液2公絲/公撮(氟可那挫) |
衛署藥製 |
043000 |
抗黴菌劑 |
滅菌靈懸液用粉劑10萬單位/毫升(耐絲菌素) |
衛署藥製 |
034904 |
預防和治療由白色念珠菌所引起之口腔、皮膚及腸內諸感染 |
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
肺癌乳癌治療劑 |
多西20毫克/毫升單支注射液 |
衛部藥製 |
058065 |
乳癌、非小細胞肺癌、前列腺癌、胃腺癌、頭頸癌。 |
欣沛方注射液6毫克/毫升 |
衛署藥製 |
045331 |
晚期卵巢癌、腋下淋巴轉移之乳癌,作為接續含杜薩魯比辛(doxorubicin)在內之輔助化學療法、已使用合併療法(除非有禁忌,至少應包括使用anthracycline抗癌藥)失敗的轉移乳癌、非小細胞肺癌、愛滋病相關卡波西氏肉瘤之第二線療復發且無法手術切除或轉移性之乳癌病患、與Herceptin併用時,用於治療未接受過化學治療之轉移性且乳癌過度表現HER乳癌法;與CISPLATIN併用,作為晚期卵巢癌之第一線療法。與GEMCITABINE併用,可使用於曾經使用過anthracycline之局部2之病人 |
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
B型肝炎治療劑 |
利甘平膜衣錠0.5毫克 |
衛部藥製 |
058091 |
治療有B型肝炎病毒複製跡象的成人慢性B型肝炎患者。 |
利甘平膜衣錠1毫克 |
衛部藥製 |
059253 |
治療有B型肝炎病毒複製跡象的成人慢性B型肝炎患者。 |
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
抗組織胺劑 |
抵敏膜衣錠5毫克 |
衛署藥製 |
049099 |
過敏性鼻炎(常年性及季節性)引起的相關症狀,緩解成人及12 歲以上兒童之慢性原發性蕁麻疹相關症狀。 |
"健亞"健敏錠10公絲(樂雷塔定) |
衛署藥製 |
042860 |
緩解過敏性鼻炎的相關症狀,如流鼻水、鼻塞、搔癢及眼睛搔癢和灼熱感。及緩解因慢性蕁麻疹及過敏性皮膚病所引起的症狀。 |
|
袪痰劑 |
樂咳痰舒長效錠75毫克 |
衛署藥製 |
046386 |
袪痰 |
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
尿失禁治療劑 |
痙鬆錠10毫克 |
衛部藥製 |
058618 |
平滑肌痙攣緩解及鎮痛 |
痙鬆錠5毫克 |
衛部藥製 |
058617 |
|
|
優合膜衣錠15毫克 |
衛署藥製 |
045700 |
因下列因素所造成的:(1)尿失禁。(2)不穩定性膀胱狀態之尿急及頻尿。造成上述狀態之因素有:甲:原因不明之膀胱不穩定性。乙:神經性膀胱迫尿肌反應過度,源自脊髓損傷(如:橫切損傷造成雙下肢癱瘓的病人。) |
|
攝護腺肥大治療劑 |
健諾心錠2公絲(甲磺酸多薩坐辛) |
衛署藥製 |
042378 |
高血壓、良性前列腺肥大 |
健諾心錠4公絲(甲磺酸多薩坐辛) |
衛署藥製 |
042874 |
高血壓、良性前列腺肥大 |
類別 |
Products Name(中文名稱) |
證別 |
證號 |
適應症 |
降血糖藥物 |
醣安錠2毫克 |
衛署藥製 |
046074 |
非胰島素依賴型(第二型)糖尿病 |
醣安安膜衣錠 |
衛部藥製 |
059300 |
治療以glimepiride或metformin單一藥物療法仍無法達到適當的血糖控制之第二型糖尿病患者,作為飲食和運動之外的輔助。不適合作第一線治療。 |
|
糖得舒錠50毫克 |
衛署藥製 |
049579 |
非胰島素依賴型糖尿病之治療 |
|
腸躁症治療劑 |
舒腸定膜衣錠50毫克 |
衛署藥製 |
057818 |
胃、十二指腸潰瘍、過敏性結腸、結腸炎、膽管運動困難。 |
膽結石溶解劑 |
"健亞"健膽舒錠100毫克(去氧熊膽酸) |
衛署藥製 |
042210 |
膽固醇系膽結石之溶解、原發性膽道肝硬化(Primary Biliary Cirrhosis, PBC)之肝功能改善 |

土地面積:11,649平方公尺 (3,530坪)廠房面積:6,617平方公尺 (2,005坪) |
健亞GMP廠之沿革:健亞以開發新藥為職志,為符合新藥開發及生產之嚴格要求,於民國86年2月斥資購買必治妥施貴寶公司座落於新竹工業區之GMP廠。 該廠於民國74年5月由施貴寶公司(Squibb)建立,並於78年7月與必治妥公司(Bristol-Myers)合併而改名為必治妥施貴寶公司(Bristol-Myers Squibb)新竹廠,迄86年7月關廠轉由健亞公司(GBL)經營,本公司除承接原廠軟、硬體及全體員工之外,並陸續更新廠房機器及設備以追求貫徹cGMP標準為目標,嚴格管理生產藥品之品質。94年11月完工的研發生產中心,使本廠朝向更高品質的目標,邁進一大步。 |
劑型研發:承如本公司成立之第一項宗旨:結合海內外先進之科技與人才研究開發新藥,提昇製藥及生物科技水準。本廠於創立之初即集全廠原BMS之人才參與公司新藥開發 ,以及臨床試驗藥物之研製;至今已研製有特色之學名藥,以及緩釋劑型藥物,領有超過40張之藥證,其中包含17項產品已經取得BA/BE認證,並已陸續量產上市。除此之外,現正進行數項改良劑型新藥之開發,並已進入準備臨床試驗之階段。 |
研發生產服務:健亞不僅生產自行研發之產品,為提高工廠產能、增加營收,亦接受業界委託代工生產之服務,首先於購廠合約即承接必治妥施貴寶公司所有原來生產產品之代工生產,並繼續接受亞培等公司產品委託代工,包括研製、協助領證、及量產上市,目前委託生產超過20項產品,由此可見健亞生產之品質及能力已廣為同業所推崇。 |
PIC/S GMP之實施:為配合政府實施cGMP之政策,並為貫徹本公司達成符合FDA cGMP標準之策略,以提昇產品品質,製造具安定性、有效性、安全性之藥品,本廠正盡全力執行 cGMP。湖口廠已於93年12月通過衛生署核准「全面完成cGMP確效作業」, 並於99年9月通過衛生署 ( PIC/S ) GMP 確效作業查核。願與業界共同探討,切磋 cGMP執行之各項問題,以共同提昇台灣製藥水準。 |
| 工廠地址:新竹縣湖口鄉新竹工業區工業一路一號 聯絡電話:(03)598-2221 ext.202 E-mail: hmchu@genovate-bio.com |
利害關係人之鑑別及溝通
健亞生物科技股份有限公司(以下稱本公司)之利害關係人包含員工、客戶、供應商及投資人等,本公司秉持與利害關係人保持良好關係,推行各項對內、對外的溝通事務,依據各利害關係人所關注項目,分別列入相關單位的職責,對於環境趨勢演變、法令修訂等亦能透過各單位合作進而因應處理。為滿足利害關係人的期待,本公司透過各種溝通方式,一方面確保相關工作達成,一方面維持溝通管道的暢通無誤,並將相關資訊回餽與經營團隊,作為日後改進或規劃之參考。
利害關係人 |
關注議題 |
溝通管道 |
114年溝通成果 |
溝通聯絡窗口 |
員工 |
薪資與福利人才培育與發展勞資關係職業安全與健康環境 |
健亞家庭日職工福利委員會員工健康檢查與保險安全衛生教育訓練內部公告系統 |
1.每年實施員工滿意度調查,了解同仁對公司制度及福利的滿意度,與其他需求的建議。114年12月已完成滿意度調查,並提報公司行政會議持續檢討改進。2.定期召開勞資會議促進勞資關係。114年已舉辧4次勞資會議。3.每年舉辦家庭日凝聚員工向心力、提升士氣及增進家屬對企業之認同感。114年09月13日於六福村主題遊樂園舉辦「童心同樂 趣六福村」親子家庭日。 |
員工聯絡窗口行政處經理:吳小姐TEL:03-5982221 #119E-mail:kellywu@genovate-bio.com |
客戶與消費者 |
產品品質與安全產品使用回饋客戶關係管理 |
工廠稽查產品上市後調查訂貨專線產品研討會產品教育訓練藥物不良反應通報 |
1.提供客戶多元溝通管道,設有申訴專線及電子信箱,由專人處理相關客訴或爭議事項;且依法繳納藥害救濟金,以保障消費者權益。2.每年不定期與各大醫院聯合舉辦產品研討會及參與醫學年會。 |
客戶聯絡窗口業務處經理:陳先生TEL:03-5982221 #378E-mail:hardwaychen@genovate-bio.com消費者聯絡窗口品保部經理:紀小姐TEL:03-5982221 #317E-mail:kerrychi @genovate-bio.com |
供應商 |
產品、設備之供應鏈供應商關係管理 |
公司年報營運概況公告聯絡電話與電子郵件信箱 |
每兩年做供應商評比,依評比結果,評定供應商等級、處理措施及評鑑頻率。114年完成供應商評鑑67家。 |
供應商聯絡窗口採購部:鐘小姐TEL:03-5982221 #209E-mail:shayonchung@genovate-bio.com |
投資人 |
財務資訊營運績效股利政策公司治理情形 |
股東會公司年報重大訊息公告營運概況公告法人說明會報章雜誌企業官方網站聯絡電話與電子郵件信箱 |
1.財務、業務相關資訊以公告、重訊或新聞稿形式定期或不定期對外發佈。2.每年舉辧法人說明會,影音及簡報檔連結路徑說明置放於公司官方網站。114年12月02日已舉辦法說會。 |
股東/投資人聯絡窗口發言人行政處資深處長:蔣維民 先生TEL:03-5982221 #118E-mail:williechiang@genovate-io.com代理發言人財務副總經理:林惠玲 小姐TEL:03-5982221 #116E-mail:annlin@genovate-bio.com |
對利害關係人之回應與責任
本公司一直堅持穩健的經營策略與財務運作,維護利害關係人的權利或利益,除設置相關部門和人員回應利害關係人所關注之議題外,積極提升企業價值和聲譽,同時致力成為產業中永續發展的優秀企業;自上櫃以來,透過股利的發放以回饋股東,維持穩健的資本規劃及財務結構,依主管機關規定應發佈的各項公告文件,均公開於公開資訊觀測站以及公司網站,近年來本公司更朝資訊透明、資訊揭露、公司治理等方向努力。
違反道德行為舉報
本公司已訂定「檢舉非法與不道德或不誠信行為案件之處理辦法」,鼓勵內部及外部人員檢舉不誠信或不當行為,檢舉案件由專人在保密機制下進行,本公司並承諾保護檢舉人不因檢舉情事而遭不當處置。
行政處:蔣維民先生
申訴信箱:williechiang@genovate-bio.com
申訴專線:03-5982221#118
稽核室:許棻茹小姐
申訴信箱:cindyhsu@genovate-bio.com
申訴專線:03-5982221#102
Tip’s:可用年度(2024)、月份(/01)、累計等關鍵字快速搜尋。
| 年度 | 營收金額(仟元) | 年度增(減)百分比(%) |
|---|---|---|
| 2026累計 | 149,981 | -15.38% |
| 2026/12 | - | - |
| 2026/11 | - | - |
| 2026/10 | - | - |
| 2026/09 | - | - |
| 2026/08 | - | - |
| 2026/07 | - | - |
| 2026/06 | - | - |
| 2026/05 | - | - |
| 2026/04 | 39,598 | -13.79% |
| 2026/03 | 33,450 | -25.94% |
| 2026/02 | 27,353 | -27.38% |
| 2026/01 | 49,580 | 2.28% |
| 2025累計 | 492,406 | -3.61% |
| 2025/12 | 36,961 | -4.45% |
| 2025/11 | 43,161 | 14.04% |
| 2025/10 | 39,279 | -5.79% |
| 2025/09 | 36,291 | -15.32% |
| 2025/08 | 37,298 | -11.00% |
| 2025/07 | 41,938 | 0.78% |
| 2025/06 | 40,677 | -3.51% |
| 2025/05 | 39,561 | -11.41% |
| 2025/04 | 45,934 | 14.59% |
| 2025/03 | 45,164 | -11.55% |
| 2025/02 | 37,665 | 17.41% |
| 2025/01 | 48,477 | -13.76% |
| 2024累計 | 510,856 | -3.34% |
| 2024/12 | 38,682 | 13.98% |
| 2024/11 | 37,846 | -8.11% |
| 2024/10 | 41,693 | -5.93% |
| 2024/09 | 42,855 | -4.20% |
| 2024/08 | 41,908 | -11.09% |
| 2024/07 | 41,613 | -7,91% |
| 2024/06 | 42,158 | -10.53% |
| 2024/05 | 44,656 | -11.81% |
| 2024/04 | 40,086 | -6.07% |
| 2024/03 | 51,064 | -2.22% |
| 2023/02 | 32,081 | -10.50% |
| 2024/01 | 56,214 | 29.20% |
| 2023累計 | 528,512 | 20.46% |
| 2023/12 | 33,939 | 19.91% |
| 2023/11 | 41,188 | -4.64% |
| 2023/10 | 44,320 | 1.21% |
| 2023/09 | 44,736 | 20.41% |
| 2023/08 | 47,136 | 21.34% |
| 2023/07 | 45,187 | 14.83% |
| 2023/06 | 47,122 | 23.08% |
| 2023/05 | 50,634 | 40.90% |
| 2023/04 | 42,675 | 24.66% |
| 2023/03 | 52,221 | 48.46% |
| 2023/02 | 35,846 | 34.82% |
| 2023/01 | 43,508 | 14.79% |
| 2022累計 | 438,759 | 1.04% |
| 2022/12 | 28,303 | -30.23% |
| 2022/11 | 43,194 | 14.48% |
| 2022/10 | 43,790 | 29.00% |
| 2022/09 | 37,153 | -5.94% |
| 2022/08 | 38,846 | -5.55% |
| 2022/07 | 39,350 | 4.79% |
| 2022/06 | 38,287 | 18.41% |
| 2022/05 | 35,936 | -2.67% |
| 2022/04 | 34,234 | 10.33% |
| 2022/03 | 35,175 | 0.69% |
| 2022/02 | 26,589 | 16.36% |
| 2022/01 | 37,902 | -17.18% |
| 2021累計 | 434,254 | -8.14% |
| 2021/12 | 40,565 | 65.50% |
| 2021/11 | 37,730 | 51.95% |
| 2021/10 | 33,946 | -19.39% |
| 2021/09 | 39,498 | -4.48% |
| 2021/08 | 41,129 | 16.39% |
| 2021/07 | 37,553 | -16.01% |
| 2021/06 | 32,335 | -30.28% |
| 2021/05 | 36,920 | -5.30% |
| 2021/04 | 31,028 | -19.76% |
| 2021/03 | 34,934 | -25.63% |
| 2021/02 | 22,851 | -44.31% |
| 2021/01 | 45,765 | -4.32% |
| 2020累計 | 472,723 | 1.50% |
| 2020/12 | 24,511 | -24.06% |
| 2020/11 | 24,831 | -36.95% |
| 2020/10 | 42,114 | 22.66% |
| 2020/09 | 41,351 | 5.45% |
| 2020/08 | 35,338 | 6.82% |
| 2020/07 | 44,710 | 18.24% |
| 2020/06 | 46,378 | 25.17% |
| 2020/05 | 38.988 | -5.75% |
| 2020/04 | 38,667 | 7.78% |
| 2020/03 | 46,974 | 19.24% |
| 2020/02 | 41,029 | 27.57% |
| 2020/01 | 47,832 | -25.03% |
| 2019年累計 | 465,756 | 2.18% |
| 2019/12 | 32,278 | 2.19% |
| 2019/11 | 39,383 | 4.08% |
| 2019/10 | 34,335 | -15.23% |
| 2019/09 | 39,213 | 9.71% |
| 2019/08 | 33,082 | -11.39% |
| 2019/07 | 37,814 | 9.75% |
| 2019/06 | 37,053 | -0.67% |
| 2019/05 | 41,368 | 3.62% |
| 2019/04 | 35,875 | 5.75% |
| 2019/03 | 39,393 | 5.98% |
| 2019/02 | 32,161 | -2.76% |
| 2019/01 | 63,802 | 12.04% |
| 2018年累計 | 455,798 | 11.64% |
| 2018/12 | 31,586 | 7.01% |
| 2018/11 | 37,838 | 12.56% |
| 2018/10 | 40,504 | 19.19% |
| 2018/09 | 35,742 | -4.76% |
| 2018/08 | 37,335 | 4.23% |
| 2018/07 | 34,455 | 12.79% |
| 2018/06 | 37,302 | -0.23% |
| 2018/05 | 39,922 | 8.20% |
| 2018/04 | 33,924 | 8.77% |
| 2018/03 | 37,169 | 1.60% |
| 2018/02 | 33,073 | 19.40% |
| 2018/01 | 56,948 | 51.70% |
| 2017年累計 | 411,203 | -0.71% |
| 2017/12 | 29,518 | -23.12% |
| 2017/11 | 33,615 | 10.25% |
| 2017/10 | 33,984 | 7.76% |
| 2017/09 | 37,528 | 9.37% |
| 2017/08 | 35,782 | -2.97% |
| 2017/07 | 30,548 | -26.06% |
| 2017/06 | 37,388 | 2.37% |
| 2017/05 | 36,895 | 17,11% |
| 2017/04 | 31,190 | 1.10% |
| 2017/03 | 36,584 | 5.48% |
| 2017/02 | 27,700 | -0.69% |
| 2017/01 | 37,539 | 1.95% |
| 2016年累計 | 411,203 | -13.90% |
| 2016/12 | 38,397 | -11.13% |
| 2016/11 | 30,490 | -26.09% |
| 2016/10 | 31,538 | -27.28% |
| 2016/09 | 34,313 | -15.35% |
| 2016/08 | 36,876 | -5.93% |
| 2016/07 | 41,346 | 12.32% |
| 2016/06 | 36,521 | 6.04% |
| 2016/05 | 31,505 | -17.07% |
| 2016/04 | 30,851 | -13.25% |
| 2016/03 | 34,683 | -2.97% |
| 2016/02 | 27,892 | -22.14% |
| 2016/01 | 36,821 | -31.41% |
| 2015年累計 | 477,596 | 0.45% |
| 2015/12 | 43,208 | 35.19% |
| 2015/11 | 41,253 | 23.42% |
| 2015/10 | 43,372 | 10.59% |
| 2015/09 | 40,536 | -0.48% |
| 2015/08 | 39,201 | -4.93% |
| 2015/07 | 36,783 | -21.55% |
| 2015/06 | 34,440 | 1.00% |
| 2015/05 | 37,991 | -19.70% |
| 2015/04 | 35,564 | -7.86% |
| 2015/03 | 35,745 | -7.94% |
| 2015/02 | 35,823 | 16.83% |
| 2015/01 | 53,680 | 2.25% |
| 2014年累計 | 475,450 | 19.75% |
| 2014/12 | 31,962 | 10.89% |
| 2014/11 | 33,426 | 7.98% |
| 2014/10 | 39,217 | 18.71% |
| 2014/09 | 40,731 | 17.73% |
| 2014/08 | 41,234 | 25.64% |
| 2014/07 | 46,888 | 16.22% |
| 2014/06 | 34,098 | 19.51% |
| 2014/05 | 47,309 | 38.36% |
| 2014/04 | 38,597 | 14.80% |
| 2014/03 | 38,826 | 13.07% |
| 2014/02 | 30,663 | 25.75% |
| 2014/01 | 52,499 | 26.81% |
| 2013年累計 | 397,042 | 13.06% |
| 2013/12 | 28,822 | -3.17% |
| 2013/11 | 30,956 | 27.94% |
| 2013/10 | 33,037 | 37.19% |
| 2013/09 | 34,597 | 6.44% |
| 2013/08 | 32,818 | 15.69% |
| 2013/07 | 40,345 | 36.80% |
| 2013/06 | 28,532 | -6.51% |
| 2013/05 | 34,192 | 9.32% |
| 2013/04 | 33,620 | 27.22% |
| 2013/03 | 34,339 | 9.74% |
| 2013/02 | 24,384 | -11.09% |
| 2013/01 | 41,400 | 15.51% |
| 2012年累計 | 351,187 | 5.99% |
| 2012/12 | 29,765 | 21.92% |
| 2012/11 | 24,195 | -7.01% |
| 2012/10 | 24,082 | 20.55% |
| 2012/09 | 32,505 | 11.42% |
| 2012/08 | 28,368 | 3.32% |
| 2012/07 | 29,492 | 9.59% |
| 2012/06 | 30,518 | 8.70% |
| 2012/05 | 31,277 | -13.73% |
| 2012/04 | 26,427 | -0.85% |
| 2012/03 | 31,290 | 2.78% |
| 2012/02 | 27,427 | 27.56% |
| 2012/01 | 35,841 | 4.00% |
1.年之數字係內部結算,未經會計師查核。
2.本公司配合主管機關法規修正,自2013年元月起,僅公告合併財報數字。
Tip’s:可用年度(105)、季度(Q1)、單一等關鍵字快速搜尋。
| 年度 | 詳細資料 |
|---|---|
| 115Q1 | |
| 114個體財報 | |
| 114Q4 | |
| 114Q3 | |
| 114Q2 | |
| 114Q1 | |
| 113個體財報 | |
| 113Q4 | |
| 113Q3 | |
| 113Q2 | |
| 113Q1 | |
| 112個體財報 | |
| 112Q4 | |
| 112Q3 | |
| 112Q2 | |
| 112Q1 | |
| 111個體財報 | |
| 111Q4 | |
| 111Q3 | |
| 111Q2 | |
| 111Q1 | |
| 110個體財報 | |
| 110Q4 | |
| 110Q3 | |
| 110Q2 | |
| 110Q1 | |
| 109個體財報 | |
| 109Q4 | |
| 109Q3 | |
| 109Q2 | |
| 109Q1 | |
| 108個體財報 | |
| 108Q4 | |
| 108Q3 | |
| 108Q2 | |
| 108Q1 | |
| 107個體財報 | |
| 107Q4 | |
| 107Q3 | |
| 107Q2 | |
| 107Q1 | |
| 106個體財報 | |
| 106Q4 | |
| 106Q3 | |
| 106Q2 | |
| 106Q1 | |
| 105個體財報 | |
| 105Q4 | |
| 105Q3 | |
| 105Q2 | |
| 105Q1 | |
| 104個體財報 | |
| 104Q4 | |
| 104Q3 | |
| 104Q2 | |
| 104Q1 | |
| 103個體財報 | |
| 103Q4 | |
| 103Q3 | |
| 103Q2 | |
| 103Q1 | |
| 102個體財報 | |
| 102Q4 | |
| 102Q3 | |
| 102Q2 | |
| 102Q1 | |
| 101單一Q4 | Download |
| 101單一Q3 | Download |
| 101單一Q2 | Download |
| 101單一Q1 | Download |
| 100單一Q4 | Download |
| 100單一Q3 | Download |
| 100單一Q2 | Download |
| 99單一Q4 | Download |
| 99單一Q2 | Download |
| 99Q4 | Download |
| 99Q2 | Download |
| 98單一Q4 | Download |
| 98單一Q2 | Download |
| 98Q4 | Download |
| 98Q2 | Download |
| 97單一Q4 | Download |
| 97單一Q2 | Download |
| 97Q4 | Download |
| 97Q2 | Download |
|
本公司已有簽約使用集保結算所「股務事務e櫃台(eCounter 平台)」受理股東採用數位簽章方式申辦股務事項,有關已開放申辦之股務事項,請連結集保結算所網址https://stockservices.tdcc.com.tw/evote/index.html 參閱「eCounter股務事務e櫃台」之揭示說明; 該平台尚未開放之其他股務電子化申辦事項,請維持現行以書面加蓋 原留印鑑方式向本公司股務代理機構(群益金鼎證券 股務代理部)申辦。 |
|
||||||
本公司股利政策係依據營運策略,短中長期投資規劃,資本預算及內外部環境變化,配合當年度之獲利狀況,由董事會擬具分配方案,經股東會決議後辦理。分配採股利平衡原則,以不低於當年度可供分配盈餘之百分之五十為股東紅利,其中現金股利不低於百分之十。 |
||||||
|
||||||
年度 |
股東會日期 |
每股股利(普通股) |
除權基準日 |
除息基準日 |
股利發放日 |
|
現金股利
|
股票股利
|
|||||
2024 |
2025/05/29 |
0.1 |
0.2 |
2025/08/20 |
2025/08/20 |
2025/09/24 |
2023 |
2024/05/31 |
0.150 |
0.3 |
2024/08/21 |
2024/08/21 |
2024/09/25 |
2022 |
05/29/2023 |
0.175 |
0 |
2023/07/14 |
2023/07/14 |
2023/08/04 |
2021 |
05/31/2022 |
0.35 |
0 |
2022/07/26 |
2022/07/26 |
2022/08/18 |
2020 |
8/10/2021 |
0.41 |
0.2 |
2021/09/18 |
2021/09/18 |
2021/10/15 |
2019 |
5/29/2020 |
0.465 |
0.2 |
2020/08/31 |
2020/08/31 |
2020/09/28 |
2018 |
5/30/2019 |
0.5 |
0.3 |
2019/07/23 |
2019/07/23 |
2019/08/21 |
2017 |
5/30/2018 |
0.8 |
0 |
– |
2018/07/12 |
2018/08/03 |
2016 |
6/23/2017 |
0.3522 |
0 |
– |
2017/08/02 |
2017/08/25 |
2015 |
5/30/2016 |
0.5 |
0 |
– |
2016/07/12 |
2016/08/05 |
2014 |
6/2/2015 |
0.5 |
0 |
– |
2015/07/13 |
2015/07/31 |
2013 |
6/10/2014 |
0.3 |
0 |
– |
2014/07/18 |
2014/08/04 |
2012 |
6/24/2013 |
0.3 |
0 |
– |
2013/07/16 |
2013/08/06 |
股東會相關資料查詢
Tip’s:可用年度(114年)、年報、議事等關鍵字快速搜尋。
| 項目 | 中文版 |
|---|---|
| 114年度-年報(113) | |
| 114年度-開會通知 | |
| 114年度-議事手冊及會議補充資料 | |
| 114年度-議事錄 | |
| 113年度-年報(112) | Download |
| 113年度-開會通知 | Download |
| 113年度-議事手冊及會議補充資料 | Download |
| 113年度-議事錄 | Download |
| 112年度-年報(111) | Download |
| 112年度-開會通知 | Download |
| 112年度-議事手冊 | Download |
| 112年度-議事錄 | Download |
| 111年度-年報(110) | Download |
| 111年度-開會通知 | Download |
| 111年度-議事手冊 | Download |
| 111年度-議事錄 | Download |
| 110年度-年報(109) | Download |
| 110年度-開會通知 | Download |
| 110年度-議事手冊 | Download |
| 110年度-議事錄 | Download |
| 109年度-年報(108) | Download |
| 109年度-開會通知 | Download |
| 109年度-議事手冊 | Download |
| 109年度-議事錄 | Download |
| 108年度-年報(107) | Download |
| 108年度-開會通知 | Download |
| 108年度-議事手冊 | Download |
| 108年度-議事錄 | Download |
| 107年度-年報(106) | Download |
| 107年度-開會通知 | Download |
| 107年度-議事手冊 | Download |
| 107年度-議事錄 | Download |
| 106年度-年報(105) | Download |
| 106年度-開會通知 | Download |
| 106年度-議事手冊 | Download |
| 106年度-議事錄 | Download |
| 105年度-年報(104) | Download |
| 105年度-開會通知 | Download |
| 105年度-議事手冊 | Download |
| 105年度-議事錄 | Download |
| 104年度-年報(103) | Download |
| 104年度-開會通知 | Download |
| 104年度-議事手冊 | Download |
| 104年度-議事錄 | Download |
| 103年度-年報(102) | Download |
| 103年度-開會通知 | Download |
| 103年度-議事手冊 | Download |
| 103年度-議事錄 | Download |
| 102年度-年報(101) | Download |
| 102年度-開會通知 | Download |
| 102年度-議事手冊 | Download |
| 102年度-議事錄 | Download |
| 101年度-年報(100) | Download |
| 101年度-開會通知 | Download |
| 101年度-議事手冊 | Download |
| 101年度-議事錄 | Download |
| 100年度-年報(099) | Download |
| 100年度-開會通知 | Download |
| 100年度-議事手冊 | Download |
| 100年度-議事錄 | Download |
股東會影音資料
項目 |
連結 |
20250529股東會 |
Click(外部連結) |
20240531股東會 |
Click(外部連結) |
20230529股東會 |
Click(外部連結) |
主要股東名單
持股比例占前十大股東,其相互間為關係人或為配偶、二親等以內之親屬關係之情形
114年08月26日
姓名 |
本人持有股份 |
配偶、未成年子女持有股份 |
利用他人名義合計持有股份 |
前十大股東相互間具有關係人或為配偶、二親等以內之親屬關係者,其名稱或姓名及關係。 |
備註 |
||||
股數 |
持股比率 |
股數 |
持股比率 |
股數 |
持股比率 |
名稱(或姓名) |
關係 |
||
行政院國家發展基金管理會 |
30,700,406 |
26.72% |
0 |
0% |
0 |
0% |
– |
– |
– |
代表人:陳綉暉 |
0 |
0% |
0 |
0% |
0 |
0% |
– |
– |
– |
代表人:黃奇英 |
0 |
0% |
0 |
0% |
0 |
0% |
– |
– |
– |
瑞安大藥廠股份有限公司 |
3,477,322 |
3.03% |
0 |
0% |
0 |
0% |
– |
– |
– |
代表人:林智暉 |
0 |
0% |
0 |
0% |
0 |
0% |
– |
– |
– |
健亞生物科技(股)公司庫藏股專戶 |
1,137,000 |
0.99% |
0 |
0% |
0 |
0% |
– |
– |
– |
林佐諺 |
637,714 |
0.56% |
0 |
0% |
0 |
0% |
– |
– |
– |
聯盛投資(股)公司 |
520,074 |
0.45% |
0 |
0% |
0 |
0% |
– |
– |
– |
代表人:鄭淑慎 |
0 |
0% |
0 |
0% |
0 |
0% |
– |
– |
– |
林綉婉 |
391,680 |
0.34% |
0 |
0% |
0 |
0% |
– |
– |
– |
符慧中 |
353,940 |
0.31% |
0 |
0% |
0 |
0% |
– |
– |
– |
蔡燦煌 |
347,459 |
0.30% |
0 |
0% |
0 |
0% |
– |
– |
– |
徐忠生 |
327,460 |
0.29% |
0 |
0% |
0 |
0% |
– |
– |
– |
顏鵬志 |
284,702 |
0.25% |
0 |
0% |
0 |
0% |
– |
– |
– |
群益金鼎證券( 股)公司
地 址:台北市敦化南路二段97號東帝士摩天大樓地下2樓
電 話:(02)27023999
網 址:http://www.capital.com.tw
服務項目:
-
股票過戶,股票質權設定、消滅,股票掛失、補發,股東姓名、地址、印鑑之登記或變更等股務處理準則所定之應辦事項的受理。
-
受理股東持有股份、配股、配息、股票發放等之查詢。
-
各種通知書之寄發、補發。
-
提供股東各種股務諮詢。
運作情形摘要說明
評估項目 |
運作情形 |
與上市上櫃公司治理實務守則差異情形及原因 |
||
是 |
否 |
摘要說明 |
||
一、公司是否依據「上市上櫃公司治理實務守則」訂定並揭露公司治理實務守則? |
V |
|
本公司已於112.03.10訂定「公司治理實務守則」,並已揭露於公司網站上。 |
尚符合守則之規範 |
二、公司股權結構及股東權益(一)公司是否訂定內部作業程序處理股東建議、疑義、糾紛及訴訟事宜,並依程序實施?(二)公司是否掌握實際控制公司之主要股東及主要股東之最終控制者名單?(三)公司是否建立、執行與關係企業間之風險控管及防火牆機制?(四)公司是否訂定內部規範,禁止公司內部人利用市場上未公開資訊買賣有價證券? |
VV |
|
(一)1.本公司依法於股東會前受理股東提案,鼓勵股東參與公司治理。2.本公司循發言人制度,即時妥善處理股東建議、疑義及糾紛等相關事宜。(二)1.本公司依股務代理提供之股東名冊,隨時掌握實際控制公司之主要股東及主要股東之最終控制者名單之情形。2.本公司對持股5%以上股東及董監事、內部人之股權異動,均隨時掌握,並依規定定期申報,公開揭露。(三)依「子公司監理作業程序」及「集團企業特定公司及關係人交易管理辦法」執行各項控管機制。(四)1.本公司業已訂定「公司治理實務守則」及「內部重大資訊處理暨防範內線交易管理作業程序」,禁止內部人利用市場上未公開資訊買賣有價證券。包括本公司內部人於獲悉公司財務報告或相關業績內容之日起之股票交易控管措施,包括(但不限於)董事不得於年度財務報告公告前三十日,和每季財務報告公告前十五日之封閉期間交易其股票。本公司已於發佈董事會開會預告通知時(30日前),提醒董事及內部人於前述封閉期間內,不得交易股票。2.本公司內部人於就任前均需簽署聲明書,確知證券交易法內線交易之禁止事項。於114.05.29董事持續進修課程中向所有內部人轉知有關內線交易之法令及案例提醒。3.另於114.09.05之All hands meeting中向員工宣導內線交易相關法令,並重申禁止利用職務關係所取得市場上無法取得的資訊來獲利。上述教育訓練共計148人次參與,合計296人時。 |
尚符合守則之規範 |
VV |
|
|||
|
|
|
|||
|
|
|
|||
三、董事會之組成及職責(一)董事會是否擬訂多元化政策、具體管理目標及落實執行?(二)公司除依法設置薪資報酬委員會及審計委員會外,是否自願設置其他各類功能性委員會?(三)公司是否訂定董事會績效評估辦法及其評估方式,每年並定期進行績效評估,且將績效評估之結果提報董事會,並運用於個別董事薪資報酬及提名續任之參考?(四)公司是否定期評估簽證會計師獨立性? |
VVVV |
|
(一)本公司「董事選任辦法」內明訂董事會組成之多元化政策,其提名選任乃就公司經營發展規模及其主要股東持股情形,衡酌實務需求,在專業背景、學經歷、誠信度及獨立性等多方考量下選任組成。有關1.半數有新藥開發或生醫產業相關背景。2.獨立董事席次逾董事席次三分之一。3.兼任公司經理人董事不宜逾董事席次三分之一之具體管理目標均落實達成。4.董事會成員多元化落實情形請參閱本年報第13~14頁。(二)本公司已成立薪資報酬委員會及審計委員會,並於113年08月成立永續暨風險管理委員會,其他功能性委員會,將視實際需要規劃設置。(三)本公司訂定「董事會暨功能性委員會績效評估辦法」,明定其評估方式,採董事會內部自評、董事成員自評、同儕評估、委任外部專業機構、專家等適當方式進行績效評估。1.董事會績效評估之衡量項目,包含五大面向:(1)對公司營運之參與程度。(2)提升董事會決策品質。(3)董事會組成與結構。(4)董事的選任及持續進修。(5)內部控制。2.董事成員(自我或同儕)之衡量項目含六大面向:(1)本公司目標與任務之掌握。(2)董事職責認知。(3)對公司營運之參與程度。(4)內部關係經營與溝通。(5)董事之專業及持續進修。(6)內部控制。3.114年間完成董事會績效評估及董事成員(自我)評估,評估結果提報115.01.27董事會核備。另委託「財團法人台北金融研究發展基金會」,辦理本公司董事會績效之外部評估,除進行書面審視外,於114.11.12執行現場實地訪評,並出具董事會績效評估報告,相關建議事項,本公司依規劃時程逐步改善中。並於薪資報酬委員會中依評核結果,作為董事薪酬及提名續任之參考。(四)本公司每年均自行評估所屬簽證會計師之獨立性與適任性,要求簽證會計師提供「超然獨立聲明書」及「審計品質指標(AQIs)」,並依指標進行評估。最近期評估情形係提報114.11.27審計委員會及114.11.27董事會審議通過;經查資誠聯合會計師事務所劉倩瑜會計師與鄭雅慧會計師,並未擔任本公司董事或經理人,也非本公司利害關係人,亦未在本公司支薪或有投資或財務利益分享關係,評估結果顯示皆符合本公司獨立性及適任性評估標準(獨立性檢查表參註1),足堪擔任本公司簽證會計師,會計師事務所並出具獨立性聲明書(獨立性聲明書參註2)。 |
尚符合守則之規範 |
四、上市上櫃公司是否配置適任及適當人數之公司治理人員,並指定公司治理主管,負責公司治理相關事務(包括但不限於提供董事、監察人執行業務所需資料、協助董事、監察人遵循法令、依法辦理董事會及股東會之會議相關事宜、製作董事會及股東會議事錄等)? |
V |
|
一、 本公司經110.11.09董事會決議通過,指派行政處蔣維民資深處長為本公司之公司治理主管乙職,自110.12.01任命生效,負責董事會、各功能性委員會及股東會議事資料之整備、運作、召開,議事錄製作及各項變更登記執行,亦安排董事進修課程,不定期宣導各項法令,提醒/協助董事、內部人遵循相關法令。二、 公司治理主管進俢情形:參閱本年報第49頁。 |
尚符合守則之規範 |
五、公司是否建立與利害關係人 (包括但不限於股東、員工、客戶及供應商等)溝通管道,及於公司網站設置利害關係人專區,並妥適回應利害關係人所切之重要企業社會責任議題? |
V |
|
本公司已依規定建立發言人制度,作為投資股東與消費客戶的溝通管道處理相關事宜,亦於公司網站設置利害關係人專區,就利害關係人之關注議題提供溝通管道及連絡窗口,並於公開資訊觀測站申報或公佈公司之營運狀況及重要訊息。 |
尚符合守則之規範 |
六、公司是否委任專業股務代辦機構辦理股東會事務? |
V |
|
委任群益金鼎證券股務代理部辦理股東會事務。 |
符合守則之規範 |
七、資訊公開(一)公司是否架設網站,揭露財務業務及公司治理資訊?(二)公司是否採行其他資訊揭露之方式(如架設英文網站、指定專人負責公司資訊之蒐集及揭露、落實發言人制度、法人說明會過程放置公司網站等)?(三)公司是否於會計年度終了後兩個月內公告並申報年度財務報告,及於規定期限前提早公告並申報第一、二、三季財務報告與各月份營運情形? |
VV |
V |
(一)本公司網站已部分揭露公司業務及研發訊息,另設有投資人專區連結公開資訊觀測站,並設有公司治理資訊,財務資訊、股東資訊、重大訊息公告,最新消息等專區供投資人及社會大眾對各項訊息之查詢。(二)本公司已架設英文網站,對於公司資訊之蒐集及揭露皆指派專人負責;發言人制度亦落實執行中。法人說明會之資料亦可於公司網站連結取得。 |
符合守則之規範 |
八、公司是否有其他有助於瞭解公司治理運作情形之重要資訊(包括但不限於員工權益、僱員關懷、投資者關係、供應商關係、利害關係人之權利、董事及監察人進修之情形、風險管理政策及風險衡量標準之執行情形、客戶政策之執行情形、公司為董事及監察人購買責任保險之情形等)? |
V |
|
(一) 本公司標舉人性之管理模式,對員工權益及勞資關係和諧極其重視,無論出勤、薪資、保險、退休,均依相關法令執行,其中加班費,勞保自付等項目,甚而優於勞基法規範。公司每年均進行員工滿意度調查及優質之健康檢查,並由特約醫護人員追蹤輔導,對員工之身心健康,職涯發展及自我實現均由人資部門審慎管理規劃。勞資關係良好。(二)本公司對於供應商、消費者、銀行等利害關係人,均提供完整資訊,保持暢通之溝通管道,尊重、維護其應有之合法權益。(三)董事會依規定於開會通知中提醒參與討論且表決者注意利益迴避相關事宜。且本公司董事皆秉持高度之自律,對於有利害關係之議案皆自行迴避。(四)公司訂有內控制度及風險評估機制,各項投資及發展計劃均經過審慎之風險評估,方才執行。亦購買各項保險來墊償公司財產、員工及第三人責任可能造成的損失。(五)本公司設有專責單位處理客戶訴願,追蹤改善,以保護消費者權益。(六)本公司依章程已就董事、監察人及經理人執行業務範圍依法應負之賠償責任為其投保責任保險,以降低並分散董事、監察人及經理人因錯誤或疏失而造成公司及股東重大損害之風險。(七)董事進俢情形:參閱本年報第49頁。 |
尚符合守則之規範 |
九、請就臺灣證券交易所股份有限公司公司治理中心最近年度發布之公司治理評鑑結果說明已改善情形,及就尚未改善者提出優先加強事項與措施:依據公司治理中心發佈之113年(第十一屆)公司治理評鑑結果,本公司評列上櫃公司排名前36%~50%區間。未來將針對評鑑結果未達標項目,持續提升及強化。 |
||||
公司治理主管進修情形 |
|||||||
|
|
就任日期 |
進修日期 |
主辦單位 |
課程名稱 |
進修時數 |
進修是否符合規定 |
|
起 |
迄 |
||||||
蔣維民 |
110.12.01 |
114.05.29 |
114.05.29 |
財團法人台北金融研究發展基金會 |
公司治理-永續報告書GRI準則 |
3 |
是 |
114.10.16 |
114.10.16 |
金融監督管理委員會 |
15屆台北公司治理論壇 |
6 |
是 |
||
114.12.03 |
114.12.03 |
中華公司治理協會 |
全球趨勢分析-風險與機會 |
3 |
是 |
||
獨立董事溝通情形
一、獨立董事與內部稽核主管及會計師之溝通政策
-
獨立董事與會計師每年至少一次之頻率會議溝通,會計師就本公司財務狀況及內控查核情形向獨立董事報告,並針對有無重大調整分錄或法令修訂有無影響帳列情形充分溝通;若遇重大異常事項時得隨時召集會議。
-
內部稽核主管於稽核報告及追蹤報告呈核董事長後,每月透過電子郵件交付各獨立董事查閱,相關意見透過郵件回覆,並每季至少一次之頻率會議溝通及回覆各獨立董事之諮詢。
二、歷次獨立董事與會計師溝通情形摘要:
日期 溝通重點 執行情形
2025/11/6
審計委員會
1.2025年第三季合併財務報告核閱與治理單位溝通事項。
2.關係人之資訊。
3.客戶聲明書。
4.會計師之獨立性。
5.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2025/11/6董事會,就2025年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
獨立董事無意見。
2025/8/5
審計委員會
1.2025年第二季合併財務報告查核與治理單位溝通事項。
2.關係人之資訊。
3.客戶聲明書。
4.會計師之獨立性。
5.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2025/8/5董事會,就2025年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
獨立董事無意見。
2025/5/8
審計委員會
1.2025年第一季合併財務報告查核與治理單位溝通事項。
2.關係人之資訊。
3.客戶聲明書。
4.會計師之獨立性。
5.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2025/5/8董事會,就2025年第一季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
獨立董事無意見。
2025/3/11
審計委員會
1.2024年度合併及個體財務報告查核與治理單位溝通事項。
2.關係人之資訊。
3.客戶聲明書。
4.會計師之獨立性。
5.近期法令更新。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2025/3/11董事會,就2024年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通。
獨立董事無意見。
2024/11/5
審計委員會 1.2024年第三季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2024/11/5董事會,就2024年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2024/8/6
審計委員會 1.2024年第二季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2024/8/6董事會,就2024年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2024/5/7
審計委員會 1.2024年第一季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2024/5/7董事會,就2024年第一季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2024/3/12
審計委員會 1.2023年度合併及個體財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2024/3/12董事會,就2023年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2023/11/7
審計委員會 1.2023年第三季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2023/11/7董事會,就2023年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2023/8/7
審計委員會 1.2023年第二季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2023/8/7董事會,就2023年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2023/5/9
審計委員會
1.2023年第一季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2023/5/9董事會,就2023年第一季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2023/3/10
審計委員會
1.2022年度合併及個體財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2023/3/10董事會,就2022年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2022/11/8
審計委員會
1.2022年第三季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2022/11/8董事會,就2022年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2022/8/9
審計委員會
1.2022年第二季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.法令更新-審計品質指標。
7.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2022/8/9董事會,就2022年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2022/5/10
審計委員會
1.2022年第一季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2022/5/10董事會,就2022年第一季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2022/3/11
審計委員會
2022/3/11
審計委員會 1.2021年度合併及個體財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2022/3/11董事會,就2021年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2021/11/09
審計委員會 1.2021年第三季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2021/11/9董事會,就2021年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2021/08/10
審計委員會 1.2021年第二季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2021/8/10董事會,就2021年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2021/05/11
審計委員會 1.2021年第一季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2021/5/11董事會,就2021年第一季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2021/03/12
審計委員會 1.2020年度合併及個體財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2021/3/12董事會,
就2020年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2020/11/09
審計委員會 1.2020年第三季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2020/11/9董事會,
就2020年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2020/08/07
審計委員會 1.2020年第二季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2020/8/7董事會,
就2020年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2020/05/07
審計委員會 1.2020年第一季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2020/5/7董事會,
就2020年第一季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2020/03/11
審計委員會 1.2019年度合併及個體財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2020/3/11董事會,
就2019年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2019/11/7
審計委員會 1.2019年第三季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2019/11/7董事會,
就2019年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2019/8/8
審計委員會 1.2019年第二季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2019/8/8董事會,就2019年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2019/5/8
審計委員會 1.2019年第一季合併財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2019/5/8董事會,就2019年第一季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2019/3/12
審計委員 1.2018年度合併及個體財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通 會計師列席2019/3/12董事會,就2018年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通
2018/11/8
審計委員會 1.2018年第三季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2018/11/8董事會,就2018年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2018/8/8
審計委員會 1.2018年第二季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2018/8/8董事會,就2018年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2018/5/9
審計委員會 1.2018年會計師與治理單位溝通時間表
2.本會計師之角色、責任及獨立性。
3.本年度之核閱/查核計畫。
4.2018年第一季合併財務報告核閱與治理單位溝通事項。
5.重大調整分錄、重分類分錄及未調整分錄。
6.關係人名單及關係人之資訊。
7.客戶聲明書。
8.會計師之獨立性。
9.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2018/5/9董事會,就2018年第一季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2018/3/14
審計委員會 1.2017年度合併及個體財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
會計師列席2018/3/14董事會,就2017年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2017/11/10
審計委員會 1.2017年第三季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2017/11/10董事會,就2017年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2017/08/09
審計委員會 1.2017年第二季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 會計師列席2017/8/9董事會,就2017年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
2017/05/09 1.2017年第一季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄及重分類分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 財務報告事項提案董事會報告
2017/04/17 1.2017年會計師與治理單位溝通時間表
2.本年度之核閱/查核計畫。
3.本會計師之角色、責任及獨立性。
4.關係人名單及關係人交易。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 依相關討論執行
2017/03/23 1.2016年度合併及個體財務報告完成階段與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 財務報告事項提案董事會報告
2016/11/08 1.2016年第三季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.風險評估與關鍵查核事項之初步看法
7.會計師針對與會人員所提問題進行討論及溝通。 財務報告事項提案董事會報告
2016/08/09 1.2016年第二季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 財務報告事項提案董事會報告
2016/05/09 1.2016年第一季合併財務報告核閱與治理單位溝通事項。
2.重大調整分錄及重分類分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。 財務報告事項提案董事會報告
2016/04/11 1.2016年會計師與治理單位溝通時間表
2.本年度之核閱/查核計畫。
3.本會計師之角色、責任及獨立性。
4.關係人名單及關係人交易。
5.重要之法令要求及風險。
6.會計師針對與會人員所提問題進行討論及溝通。 依相關討論執行
2016/03/14 1.2015年度合併及個體財務報告完成階段與治理單位溝通事項。
2.重大調整分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
財務報告事項提案董事會報告
審計委員會
2.關係人之資訊。
3.客戶聲明書。
4.會計師之獨立性。
5.會計師針對與會人員所提問題進行討論及溝通。
獨立董事無意見。
審計委員會
2.關係人之資訊。
3.客戶聲明書。
4.會計師之獨立性。
5.會計師針對與會人員所提問題進行討論及溝通。
獨立董事無意見。
審計委員會
2.關係人之資訊。
3.客戶聲明書。
4.會計師之獨立性。
5.會計師針對與會人員所提問題進行討論及溝通。
獨立董事無意見。
審計委員會
2.關係人之資訊。
3.客戶聲明書。
4.會計師之獨立性。
5.近期法令更新。
6.會計師針對與會人員所提問題進行討論及溝通。
獨立董事無意見。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.法令更新-審計品質指標。
7.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
審計委員會 1.2021年度合併及個體財務報告查核與治理單位溝通事項。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
就2020年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
就2020年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
就2020年第二季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
就2020年第一季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
就2019年度合併及個體財務報告情形進行說明並就與董事所提問題進行討論與溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
就2019年第三季合併財務報告情形進行說明並就與董事所提問題進行討論與溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.本會計師之角色、責任及獨立性。
3.本年度之核閱/查核計畫。
4.2018年第一季合併財務報告核閱與治理單位溝通事項。
5.重大調整分錄、重分類分錄及未調整分錄。
6.關係人名單及關係人之資訊。
7.客戶聲明書。
8.會計師之獨立性。
9.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
審計委員會
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
2.重大調整分錄及重分類分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
2.本年度之核閱/查核計畫。
3.本會計師之角色、責任及獨立性。
4.關係人名單及關係人交易。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.風險評估與關鍵查核事項之初步看法
7.會計師針對與會人員所提問題進行討論及溝通。
2.重大調整分錄、重分類分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
2.重大調整分錄及重分類分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
2.本年度之核閱/查核計畫。
3.本會計師之角色、責任及獨立性。
4.關係人名單及關係人交易。
5.重要之法令要求及風險。
6.會計師針對與會人員所提問題進行討論及溝通。
2.重大調整分錄及未調整分錄。
3.關係人之資訊。
4.客戶聲明書。
5.會計師之獨立性。
6.會計師針對與會人員所提問題進行討論及溝通。
三、歷次獨立董事與內部稽核主管溝通情形摘要:
日期 溝通重點 執行情形
2025/11/06
審計委員會
1.2025年07月至2025年09月稽核業務執行報告。
2.2025年度稽核計畫。
3.修正本公司內控辦法「人力資源管理作
業」案。
1. & 2. 獨立董事無意見,提報董事會決議。
3.經主席徵詢與會委員,獨立董事提議修正案由敘述為:修正本公司內控辦法「人力資源管理作業」及相關內部稽核作業程序與稽核重點案。同意依修正案通過,提報董事會討論。
2025/09/30
審計委員會
1.修訂本公司「取得或處分資產處理程序」案。 獨立董事無意見,提報董事會決議。
2025/08/05
審計委員會
1.2025年04月至2025年06月稽核業務執行報告。 獨立董事無意見,提報董事會核備。
2025/05/08
審計委員會
1.2025年02月至2025年03月稽核業務執行報告。
2.修訂本公司「集團企業、特定公司及關係人交易管理辦法」案。
獨立董事無意見,提報董事會核備。
2025/03/11
審計委員會
1.2024年10月至2025年01月稽核業務執行報告。
2.2024年內部控制制度有效性考核及內部控制制度聲明書。
獨立董事無意見,提報董事會決議。
2024/11/05
審計委員會 1.2024年07月至2024年09月稽核業務執行報告。
2.2025年度稽核計畫。
3.訂定本公司「永續資訊管理作業辦法」。
4.訂定本公司「永續報告書編製及確信之作業程序」。
5.修正本公司「銷貨及收款管理」。 獨立董事無意見,提報董事會決議。
2024/08/06
審計委員會 1.2024年04月至2024年06月稽核業務執行報告。 獨立董事無意見,提報董事會核備。
2024/05/07
審計委員會 1.2024年02月至2024年03月稽核業務執行報告。 獨立董事無意見,提報董事會核備。
2024/03/12
審計委員會 1.2023年10月至2024年01月稽核業務執行報告。
2.2023年內部控制制度有效性考核及內部控制制度聲明書。 獨立董事無意見,提報董事會決議。
2023/11/07
審計委員會
1.2023年07月至2023年09月稽核業務執行報告。
2.民國113年度稽核計畫。
獨立董事無意見,提報董事會決議。
2023/08/07
審計委員會
1.2023年04月至2023年06月稽核業務執行報告。 獨立董事無意見,提報董事會決議。
2023/05/09
審計委員會
1.2023年02月至2023年03月稽核業務執行報告。 獨立董事無意見,提報董事會決議。
2023/03/10
審計委員會
1.2022年10月至2023年1月稽核業務執行報告。
2.111年內部控制制度有效性考核及內部控制制度聲明書。
3.修訂本公司「內部重大資訊處理暨防範內線交易管理作業程序」案。
獨立董事無意見,提報董事會決議。
2022/11/08
審計委員會 1.2022年07月至2022年09月稽核業務執行報告
2.民國112年度稽核計畫
3.修正本公司內部控制制度及內部稽核實施細則案 獨立董事無意見,提報董事會決議。
2022/08/09
審計委員會 1.2022年04月至2022年06月稽核業務執行報告 獨立董事無意見,提報董事會核備。
2022/05/10
審計委員會 1.2022年02月至2022年03月稽核業務執行報告 獨立董事無意見,提報董事會核備。
2022/03/11
審計委員會 1.2021年10月至2022年1月稽核業務執行報告
2.110年內部控制制度有效性考核及內部控制制度聲明書
3.修訂本公司「取得或處分資產處理程序」案 獨立董事無意見,提報董事會決議。
2021/12/17
審計委員會 1.修正本公司「董事會議事運作之稽核」內部稽核實施細則案 獨立董事無意見,提報董事會決議。
2021/11/09
審計委員會 1.2021年7月至2021年9月稽核業務執行報告。
2.修正本公司內部控制制度及內部稽核實施細則案
獨立董事無意見,提報董事會決議。
2021/08/10
審計委員會 1.2021年4月至2021年6月稽核業務執行報告。 獨立董事無意見,提報董事會決議。
2021/05/11
審計委員會 1.2021年2月至2021年3月稽核業務執行報告。 獨立董事無意見,提報董事會決議。
2021/03/12
審計委員會 1.2020年10月至2021年1月稽核業務執行報告。
2.109年內部控制制度有效性考核及內部控制制度聲明書 獨立董事無意見,提報董事會決議。
2020/11/09
審計委員會 1.2020年6月至9月稽核業務執行報告
2.民國110年度稽核計畫 獨立董事無意見,提報董事會決議。
2020/08/07
審計委員會 1.2020年4月至5月稽核業務執行報告
2.修訂本公司「研發作業管理」 獨立董事無意見,提報董事會決議。
2020/05/07
審計委員會 1.2020年2月至3月稽核業務執行報告 獨立董事無意見,提報董事會決議。
2020/03/11
審計委員會 1.2019年10月至2020年1月稽核業務執行報告
2.108年內部控制制度有效性考核及內部控制制度聲明書 獨立董事無意見,提報董事會決議。
2019/11/07
審計委員會
1.2019年7月至9月稽核業務執行報告
2.修訂本公司「審計委員會組織規程」
3. 民國109年度稽核計畫 獨立董事無意見,提報董事會決議。
2019/08/08
審計委員會
1.2019年4月至6月稽核業務執行報告 獨立董事無意見,提報董事會決議。
2019/05/08
審計委員會
1.2019年2月至3月稽核業務執行報告
2.修訂本公司「資金貸與他人作業程序」
獨立董事無意見,提報董事會決議。
2019/03/12
審計委員會
1.2018年11月至2019年1月稽核業務執行報告
2.107年內部控制制度有效性考核及內部控制制度聲明書
3.修訂本公司「取得或處分資產處理程序(含衍生商品)」
4.修訂本公司「背書保證施行作業程序」
獨立董事無意見,提報董事會決議。
2018/12/17
審計委員會 1.2018年10月稽核業務執行報告 獨立董事無意見,提報董事會決議。
2018/11/8
審計委員會 1.2018年7月至9月稽核業務執行報告
2.民國108年度稽核計畫 獨立董事無意見,提報董事會決議。
2018/8/8
審計委員會 1.2018年4月至6月稽核業務執行報告 獨立董事無意見,提報董事會決議。
2018/5/9
審計委員會 1.2018年2月至3月稽核業務執行報告 2. 修訂本公司內部控制制度 獨立董事無意見,提報董事會決議。
2018/3/14
審計委員會 1.2017年11月至2018年1月稽核業務執行報告
2.107年內部控制制度有效性考核及內部控制制度聲明書 獨立董事無意見,提報董事會決議。
2017/12/20
審計委員會 1.2017年10月稽核業務執行報告
2.民國106年度稽核計畫變更
3.修訂本公司內部控制制度及內部稽核實施細則
4.民國107年稽核計畫 獨立董事無意見,提報董事會決議。
2017/11/10 1.2017年9月稽核業務執行報告
2.修訂本公司「審計委員會組織規程」 獨立董事無意見,提報董事會決議。
2017/09/18 2017年7月至8月稽核業務執行報告 提案董事會報告
2017/08/09 1.2017年6月稽核業務執行報告 2.修訂本公司內部控制制度 3.修訂本公司「取得或處分資產處理程序」 提案董事會報告
2017/07/05 2017年4月至5月稽核業務執行報告 提案董事會報告
2017/05/09 2017年2月至3月稽核業務執行報告 提案董事會報告
2017/03/23 2016年11月至2017年1月稽核業務執行報告 提案董事會報告
2016/12/23 2016年10月稽核業務執行報告 提案董事會報告
2016/11/08 2016年7月至9月稽核業務執行報告 提案董事會報告
2016/08/09 2016年5月至6月稽核業務執行報告 提案董事會報告
2016/05/31 2016年4月稽核業務執行報告 提案董事會報告
2016/05/09 2016年2月至3月稽核業務執行報告 提案董事會報告
2016/03/04 2015年12月至2016年1月稽核業務執行報告。 提案董事會報告
審計委員會
2.2025年度稽核計畫。
3.修正本公司內控辦法「人力資源管理作
業」案。
3.經主席徵詢與會委員,獨立董事提議修正案由敘述為:修正本公司內控辦法「人力資源管理作業」及相關內部稽核作業程序與稽核重點案。同意依修正案通過,提報董事會討論。
審計委員會
審計委員會
審計委員會
2.修訂本公司「集團企業、特定公司及關係人交易管理辦法」案。
審計委員會
2.2024年內部控制制度有效性考核及內部控制制度聲明書。
審計委員會
2.2025年度稽核計畫。
3.訂定本公司「永續資訊管理作業辦法」。
4.訂定本公司「永續報告書編製及確信之作業程序」。
5.修正本公司「銷貨及收款管理」。
審計委員會
審計委員會
審計委員會
2.2023年內部控制制度有效性考核及內部控制制度聲明書。
審計委員會
2.民國113年度稽核計畫。
審計委員會
審計委員會
審計委員會
2.111年內部控制制度有效性考核及內部控制制度聲明書。
3.修訂本公司「內部重大資訊處理暨防範內線交易管理作業程序」案。
審計委員會
2.民國112年度稽核計畫
3.修正本公司內部控制制度及內部稽核實施細則案
審計委員會
審計委員會
審計委員會
2.110年內部控制制度有效性考核及內部控制制度聲明書
3.修訂本公司「取得或處分資產處理程序」案
審計委員會
審計委員會
2.修正本公司內部控制制度及內部稽核實施細則案
審計委員會
審計委員會
審計委員會
2.109年內部控制制度有效性考核及內部控制制度聲明書
審計委員會
2.民國110年度稽核計畫
審計委員會
2.修訂本公司「研發作業管理」
審計委員會
審計委員會
2.108年內部控制制度有效性考核及內部控制制度聲明書
審計委員會
2.修訂本公司「審計委員會組織規程」
3. 民國109年度稽核計畫
審計委員會
審計委員會
2.修訂本公司「資金貸與他人作業程序」
審計委員會
2.107年內部控制制度有效性考核及內部控制制度聲明書
3.修訂本公司「取得或處分資產處理程序(含衍生商品)」
4.修訂本公司「背書保證施行作業程序」
審計委員會
審計委員會
2.民國108年度稽核計畫
審計委員會
審計委員會
審計委員會
2.107年內部控制制度有效性考核及內部控制制度聲明書
審計委員會
2.民國106年度稽核計畫變更
3.修訂本公司內部控制制度及內部稽核實施細則
4.民國107年稽核計畫
2.修訂本公司「審計委員會組織規程」
推動誠信經營情形
本公司指派行政處為推動企業誠信經營專職單位,並由該部門每年定期向董事會報告其執行情形。
公司依「上市上櫃公司誠信經營守則」及相關法令之規範,執行各項誠信經營之措施:
-
制定誠信經營之各項規範:公司已完成「誠信經營守則」、「誠信經營作業程序及行為指南」、「道德行為準則」之制定,並公布於公司公共之資訊系統中,具體述明及規範董事,經理人及員工於從事商業行為過程中之行為準則,以避免發生違反誠信、不法或違背受託義務等不誠信行為。
-
由行政處負責推動實踐,本(114)年度於114.09.05 All hands meeting,宣導公司誠信經營之理念及創新、合作、共榮之企業文化及價值觀,正確傳達員工從事各項事務時,應遵守之行為準則及道德標準,強調不得直接或間接提供、收受、承諾或要求任何不正當利益,或從事其他違反誠信、不法或違背受託義務之行為;並揭示檢舉制度作業程序及保密機制。
上述教育訓練共計148人次參與,合計296人時。
-
依「檢舉非法與不道德或不誠信行為案件之處理方法」,設置意見箱,公布檢舉郵件信箱及檢舉專案人員電話,宣導檢舉流程及注意事項,期能及時杜絕非法與不誠信或不道德之行為。
行政處:蔣維民先生
申訴信箱:williechiang@genovate-bio.com
申訴專線:03-5982221#118
稽核室:許棻茹小姐
申訴信箱:cindyhsu@genovate-bio.com
申訴專線:03-5982221#102
-
落實執行各項內控制度:時時檢討改進,建立有效的會計制度及內控制度,由獨立之內部稽核單位定期查核,並提報董事會追蹤改進。
-
本公司與他人簽訂契約,其內容包含遵守誠信經營政策及交易相對人如涉及不誠信行為,得隨時終止或解除契約之條款。
-
誠信經營推動情形資訊接露:公司於公開資訊觀測站揭露「誠信經營守則」、「誠信經營作業程序及行為指南」、「道德行為準則」等相關規範,並以年報揭露誠信經營相關資訊。
-
本公司董事長身兼交易對手(利害關係人)之負責人,為避免涉及有自身利害關係致損於公司利益之虞,故本公司將關係人間(董事長同為一人)簽訂之有效合約報請董事會審議核備。
-
本公司各項公益贊助/捐贈,均依相關法令、公司政策及內部作業程序執行,杜絕變相行賄弊端。
-
114年誠信經營推動情形,已彙整於114.12.17向董事會報告。
董事會權責
一、公司之營運計畫。
二、年度財務報告及半年度財務報告。但半年度財務報告依法令規定無需經
會計師查核簽證者,不在此限。
三、訂定或修正內部控制制度。
四、訂定或修正取得或處分資產、從事衍生性商品交易、資金貸與他人、為他人背書或提供保證之重大財務業務行為之處理程序。
五、募集、發行或私募具有股權性質之有價證券。
六、財務、會計或內部稽核主管之任免。
七、對關係人之捐贈或對非關係人之重大捐贈。但因重大天然災害所為急難救助之公益性捐贈,得提下次董事會追認。
八、依證券交易法第十四條之三、其他依法令或章程規定應由股東會決議或董事會決議事項或主管機關規定之重大事項。
董事會成員
職稱
姓名
主要經(學)歷
目前兼任本公司及其他公司之職務
董事
陳正
.美國羅徹斯特大學化學博士
.諾華計劃主持人
.Genelabs亞洲業務副總裁
.華鼎生技顧問(股)公司董事長
.行政院生技產業策略諮議委員會(BTC)委員
.健亞生物科技(股)公司董事長兼策略長
.昌達生化科技(股)公司法人代表(董事)
.Genovate Biotechnology(Cayman) Co., Ltd. 法人代表(董事)
.華宇藥品(股)公司董事長兼策略長
.瑞寶基因(股)公司法人代表(董事)
.浩宇生醫(股)公司法人代表(董事長)兼策略長
.Genovate NaviFus (Australia)Pty.Ltd.法人代表(董事)
.松瑞製藥(股)公司法人代表(董事)
董事
陳綉暉
.台灣大學農業化學研究所 博士
.生物技術開發中心執行長室主任
、企劃管考室主任、研發處研究員
.宜誠生物科技研究員
.中央研究院博士後研究員
.生物技術開發中心副執行長
.台康生技法人代表(董事)
董事
黃奇英
.美國愛荷華州立大學生物化學及生物物理學 博士
.智擎生技製藥(股)公司董事
.國家衛生研究院副研究員
.美國史丹佛大學化學與系統生物學系 博士後研究員
.陽明交通大學生物藥學研究所特聘教授兼所長
.高雄醫學大學生物化學科合聘教授
.益得生物科技股份有限公司法人代表(董事)
董事
朱佳真
.美國哈佛大學醫療政策與管理 碩士
.健亞生物科技(股)公司國際事務處長
.健亞生物科技(股)公司新藥開發事業副總經理
.健亞生物科技(股)公司總經理
.華宇藥品(股)公司法人代表(董事)
.浩宇生醫(股)公司法人代表(董事)
.Genovate NaviFus Inc.法人代表(董事)
.Genovate NaviFus (Australia)Pty.Ltd.
法人代表(董事)
獨立
董事
李世仁
.美國南加大化學 博士
.易威生醫科技(股)公司董事長
.浩理生技管理顧問(股)公司董事總經理
.合裕管理顧問股份有限公司投資長
.Silver Biotech Management, Inc. Managing Director
.中華開發工業銀行投資部資深協理
.全崴生技(股)公司董事長
.泰合生技藥品(股)公司董事長
.三晃(股)公司獨立董事
.中裕新藥(股)公司獨立董事
.浩鼎生技(股)公司獨立董事
.創新工業技術移轉(股)公司董事
.Amphastar Pharmaceuticals,Inc董事(California US)
.CapsoVision,Inc.董事(California US)
獨立
董事
劉克宜
.廈門大學會計博士
.美國伊利諾大學會計碩士
.國立政治大學財稅學士
.會計研究發展基金會審計準則委員會委員
.中華民國會計師公會全國聯合會理事
.立本台灣聯合會計師事務所合夥會計師
.合作金庫金融控股股份有限公司獨立董事
獨立
董事
張金明
.美國德州大學奧斯汀分校藥學 博士,國立台灣大學藥學系畢業
.美國愛力根公司(Allergan Inc.)藥品,製程、及技術開發高階資深主管
.美國禮來藥廠(Eli Lilly & Company)資深研究員
.中裕新藥(股)公司執行長
.美國Biotheravision Inc.董事
.中國欧科健生物医药科技有限公司董事
健亞生物科技股份有限公司
董事會成員多元化政策
一、董事會多元化:
A.公司於「董事選任辦法」中明訂董事會組成之多元化原則及強化公司治理並促進董事會組成結構之健全發展;董事選舉提名採候選人提名制,經董事會決議通過後送請股東會選任之。就本身運作、營運型態及發展需求以擬訂適當之多元化方針,宜包括但不限於以下二大面向之標準:
a.基本條件與價值:性別、年齡、國籍及文化等。
b.專業知識技能:專業背景(如法律、會計、產業、財務、行銷或科技)、專業技能、產業經驗、經營管理、國際觀及領導決策力等。
B.多元化政策管理目標:本公司所營之醫藥研發/生產業別屬高度專業及技術導向之屬性,因此設定董事需過半數有相關產業經驗(如新藥研發、藥品開發、醫藥生產管理、醫藥市場行銷/投資…等),本公司現任8席董事,具體管理目標即達成情形如下:
管理目標
達成情形
半數有新藥開發或生醫產業相關背景
6席具產業背景,達成。
獨立董事席次逾董事席次三分之一
3席獨董,達成。
兼任公司經理人董事不宜逾董事席次三分之一
2席兼任公司經理人,達成。
C.落實執行情形
a.多元化核心項目執行情形表
多元化
核心項目
董事姓名
性別
國籍
專業資格與經驗
營運
判斷
財務
會計
經營
管理
危機
處理
產業
知識
國際觀
領導
決策
陳綉暉
女
本國
五年以上公司業務所需經驗,具生技新藥開發、技術、產業聯盟等實務專才,現為財團法人生物技術開發中心代理執行長。
未有公司法第30條各款情事之一。
V
V
V
V
V
V
V
黃奇英
男
本國
五年以上公司業務所需經驗,現為陽明交通大學藥科院副院長,專長為新藥及中草藥之研發,建立老藥新用藥物篩選平台,產學合作經驗豐富。
未有公司法第30條各款情事之一。
V
V
V
V
V
V
V
陳 正
男
本國
具有五年以上公司業務所需之工作經驗,具跨國醫藥研發及公司經營管理專才;曾任美國Genelabs Technologies.亞洲業務副總裁,現任本公司董事長兼策略長。未有公司法第30條各款情事之一。
V
V
V
V
V
V
V
朱佳真
女
本國
具有五年以上公司業務所需之工作經驗,具醫藥研發及公司經營管理專才
;歷任本公司新藥研發及國際事務相關要職,現任本公司總經理。未有公司法第30條各款情事之一。
V
V
V
V
V
V
V
獨立董事
李世仁
男
本國
具有五年以上公司業務所需之工作經驗,具國際產業投資及公司經營管理專才;曾任浩理生技管理顧問公司董事總經理,現為國內多家生技公司(全葳、泰合、易威)董事長或董事。未有公司法第30條各款情事之一。
V
V
V
V
V
V
V
獨立董事
劉克宜
女
本國
具有五年以上公司業務所需之工作經驗,美國伊利諾大學會計碩士,中華民國簽證會計師,現為立本台灣聯合會計師事務所合夥會計師。未有公司法第30條各款情事之一。
V
V
V
V
V
V
V
獨立董事
張金明
男
本國
具有五年以上公司業務所需之工作經驗,台大藥學系畢及美國德州大學藥學博士,於美國大藥廠Eli Lilly 、Allergan工作超過20年,擔任研發主管,掌理跨國業務,熟悉小分子藥物之開發,產業經驗豐富,
現為中裕新藥執行長。未有公司法第30條各款情事之一。
V
V
V
V
V
V
V
b.本公司112年05月29股東會完成董事改選(含獨立董事3席),及113年05月31日增選獨立董事1席,(獨立董事共4席)。成員包含醫藥專業、經營管理、商務會計、投資評估等專業人士,組成背景多元。
分析如下:
․具員工身份董事佔比:2/7
․獨立董事佔比:3/7
․女性董事佔比:3/7
․產業經驗/專業人仕佔比:6/7
c.獨立董事任期年資 人數
獨立董事任期年資
人數
1 ~ 3年
1
4 ~ 6年
0
7 ~ 9年
1
大於9年
1
d.董事年齡分佈:
董事年齡
人數
31 ~ 40歲
0
41 ~ 50歲
0
51 ~ 60歲
5
61 ~ 70歲
2
71 ~ 80歲
0
董事會權責
一、公司之營運計畫。
二、年度財務報告及半年度財務報告。但半年度財務報告依法令規定無需經 會計師查核簽證者,不在此限。
三、訂定或修正內部控制制度。
四、訂定或修正取得或處分資產、從事衍生性商品交易、資金貸與他人、為他人背書或提供保證之重大財務業務行為之處理程序。
五、募集、發行或私募具有股權性質之有價證券。
六、財務、會計或內部稽核主管之任免。
七、對關係人之捐贈或對非關係人之重大捐贈。但因重大天然災害所為急難救助之公益性捐贈,得提下次董事會追認。
八、依證券交易法第十四條之三、其他依法令或章程規定應由股東會決議或董事會決議事項或主管機關規定之重大事項。
董事會成員
職稱 |
姓名 |
主要經(學)歷 |
目前兼任本公司及其他公司之職務 |
董事 |
陳正 |
.美國羅徹斯特大學化學博士.諾華計劃主持人.Genelabs亞洲業務副總裁.華鼎生技顧問(股)公司董事長.行政院生技產業策略諮議委員會(BTC)委員 |
.健亞生物科技(股)公司董事長兼策略長.昌達生化科技(股)公司法人代表(董事).Genovate Biotechnology(Cayman) Co., Ltd. 法人代表(董事).華宇藥品(股)公司董事長兼策略長.瑞寶基因(股)公司法人代表(董事).浩宇生醫(股)公司法人代表(董事長)兼策略長.Genovate NaviFus (Australia)Pty.Ltd.法人代表(董事).松瑞製藥(股)公司法人代表(董事) |
董事 |
陳綉暉 |
.台灣大學農業化學研究所 博士.生物技術開發中心執行長室主任、企劃管考室主任、研發處研究員.宜誠生物科技研究員.中央研究院博士後研究員 |
.生物技術開發中心副執行長.台康生技法人代表(董事) |
董事 |
黃奇英 |
.美國愛荷華州立大學生物化學及生物物理學 博士.智擎生技製藥(股)公司董事.國家衛生研究院副研究員.美國史丹佛大學化學與系統生物學系 博士後研究員 |
.陽明交通大學生物藥學研究所特聘教授兼所長.高雄醫學大學生物化學科合聘教授.益得生物科技股份有限公司法人代表(董事) |
董事 |
朱佳真 |
.美國哈佛大學醫療政策與管理 碩士.健亞生物科技(股)公司國際事務處長.健亞生物科技(股)公司新藥開發事業副總經理 |
.健亞生物科技(股)公司總經理.華宇藥品(股)公司法人代表(董事).浩宇生醫(股)公司法人代表(董事).Genovate NaviFus Inc.法人代表(董事).Genovate NaviFus (Australia)Pty.Ltd.法人代表(董事) |
獨立董事 |
李世仁 |
.美國南加大化學 博士.易威生醫科技(股)公司董事長.浩理生技管理顧問(股)公司董事總經理.合裕管理顧問股份有限公司投資長.Silver Biotech Management, Inc. Managing Director.中華開發工業銀行投資部資深協理 |
.全崴生技(股)公司董事長.泰合生技藥品(股)公司董事長.三晃(股)公司獨立董事.中裕新藥(股)公司獨立董事.浩鼎生技(股)公司獨立董事.創新工業技術移轉(股)公司董事.Amphastar Pharmaceuticals,Inc董事(California US).CapsoVision,Inc.董事(California US) |
獨立董事 |
劉克宜 |
.廈門大學會計博士.美國伊利諾大學會計碩士.國立政治大學財稅學士.會計研究發展基金會審計準則委員會委員.中華民國會計師公會全國聯合會理事 |
.立本台灣聯合會計師事務所合夥會計師.合作金庫金融控股股份有限公司獨立董事 |
獨立董事 |
張金明 |
.美國德州大學奧斯汀分校藥學 博士,國立台灣大學藥學系畢業.美國愛力根公司(Allergan Inc.)藥品,製程、及技術開發高階資深主管.美國禮來藥廠(Eli Lilly & Company)資深研究員 |
.中裕新藥(股)公司執行長.美國Biotheravision Inc.董事.中國欧科健生物医药科技有限公司董事 |
健亞生物科技股份有限公司
董事會成員多元化政策
一、董事會多元化:
A.公司於「董事選任辦法」中明訂董事會組成之多元化原則及強化公司治理並促進董事會組成結構之健全發展;董事選舉提名採候選人提名制,經董事會決議通過後送請股東會選任之。就本身運作、營運型態及發展需求以擬訂適當之多元化方針,宜包括但不限於以下二大面向之標準:
a.基本條件與價值:性別、年齡、國籍及文化等。
b.專業知識技能:專業背景(如法律、會計、產業、財務、行銷或科技)、專業技能、產業經驗、經營管理、國際觀及領導決策力等。
B.多元化政策管理目標:本公司所營之醫藥研發/生產業別屬高度專業及技術導向之屬性,因此設定董事需過半數有相關產業經驗(如新藥研發、藥品開發、醫藥生產管理、醫藥市場行銷/投資…等),本公司現任8席董事,具體管理目標即達成情形如下:
管理目標 |
達成情形 |
半數有新藥開發或生醫產業相關背景 |
6席具產業背景,達成。 |
獨立董事席次逾董事席次三分之一 |
3席獨董,達成。 |
兼任公司經理人董事不宜逾董事席次三分之一 |
2席兼任公司經理人,達成。 |
C.落實執行情形
a.多元化核心項目執行情形表
多元化核心項目董事姓名 |
性別 |
國籍 |
專業資格與經驗 |
營運判斷 |
財務會計 |
經營管理 |
危機處理 |
產業知識 |
國際觀 |
領導 |
決策 |
陳綉暉 |
女 |
本國 |
五年以上公司業務所需經驗,具生技新藥開發、技術、產業聯盟等實務專才,現為財團法人生物技術開發中心代理執行長。未有公司法第30條各款情事之一。 |
V |
|
V |
V |
V |
V |
V |
V |
黃奇英 |
男 |
本國 |
五年以上公司業務所需經驗,現為陽明交通大學藥科院副院長,專長為新藥及中草藥之研發,建立老藥新用藥物篩選平台,產學合作經驗豐富。未有公司法第30條各款情事之一。 |
V |
|
V |
V |
V |
V |
V |
V |
陳 正 |
男 |
本國 |
具有五年以上公司業務所需之工作經驗,具跨國醫藥研發及公司經營管理專才;曾任美國Genelabs Technologies.亞洲業務副總裁,現任本公司董事長兼策略長。未有公司法第30條各款情事之一。 |
V |
V |
V |
V |
V |
V |
V |
|
朱佳真 |
女 |
本國 |
具有五年以上公司業務所需之工作經驗,具醫藥研發及公司經營管理專才;歷任本公司新藥研發及國際事務相關要職,現任本公司總經理。未有公司法第30條各款情事之一。 |
V |
V |
V |
V |
V |
V |
V |
|
獨立董事李世仁 |
男 |
本國 |
具有五年以上公司業務所需之工作經驗,具國際產業投資及公司經營管理專才;曾任浩理生技管理顧問公司董事總經理,現為國內多家生技公司(全葳、泰合、易威)董事長或董事。未有公司法第30條各款情事之一。 |
V |
V |
V |
V |
V |
V |
V |
|
獨立董事劉克宜 |
女 |
本國 |
具有五年以上公司業務所需之工作經驗,美國伊利諾大學會計碩士,中華民國簽證會計師,現為立本台灣聯合會計師事務所合夥會計師。未有公司法第30條各款情事之一。 |
V |
V |
V |
V |
V |
V |
V |
|
獨立董事張金明 |
男 |
本國 |
具有五年以上公司業務所需之工作經驗,台大藥學系畢及美國德州大學藥學博士,於美國大藥廠Eli Lilly 、Allergan工作超過20年,擔任研發主管,掌理跨國業務,熟悉小分子藥物之開發,產業經驗豐富,現為中裕新藥執行長。未有公司法第30條各款情事之一。 |
V |
V |
V |
V |
V |
V |
V |
b.本公司112年05月29股東會完成董事改選(含獨立董事3席),及113年05月31日增選獨立董事1席,(獨立董事共4席)。成員包含醫藥專業、經營管理、商務會計、投資評估等專業人士,組成背景多元。
分析如下:
․具員工身份董事佔比:2/7
․獨立董事佔比:3/7
․女性董事佔比:3/7
․產業經驗/專業人仕佔比:6/7
c.獨立董事任期年資 人數
獨立董事任期年資 |
人數 |
1 ~ 3年 |
1 |
4 ~ 6年 |
0 |
7 ~ 9年 |
1 |
大於9年 |
1 |
d.董事年齡分佈:
董事年齡 |
人數 |
31 ~ 40歲 |
0 |
41 ~ 50歲 |
0 |
51 ~ 60歲 |
5 |
61 ~ 70歲 |
2 |
71 ~ 80歲 |
0 |
審計委員會
本公司於民國106年6月設置審計委員會,審計委員會應履行下列職權,並將所提建議提交董事會討論。
一、依證交法第十四條之一規定訂定或修正內部控制制度。
二、內部控制制度有效性之考核。
三、依證交法第三十六條之一規定訂定或修正取得或處分資產、從事衍生性商品交易、資金貸與他人、為他人背書或提供保證之重大財務業務行為之處理程序。
四、涉及董事自身利害關係之事項。
五、重大之資產或衍生性商品交易。
六、重大之資金貸與、背書或提供保證。
七、募集、發行或私募具有股權性質之有價證券。
八、簽證會計師之委任、解任或報酬。
九、財務、會計或內部稽核主管之任免。
十、每季財務報告及年度財務報告。
十一、其他公司或主管機關規定之重大事項。
薪酬委員會
董事會依中華民國證券交易法設置薪資報酬委員會。根據中華民國證券法規,薪資報酬委員會應至少包含一席符合中華民國證券法規定義之獨立董事。薪資報酬委員會目前有三位成員,均為獨立董事。
根據董事會通過之薪資報酬委員會組織規程,薪資報酬委員會負責建立與審核有關董事與經理人績效評估與薪酬的政策、制度、標準及結構,並且評估董事與經理人的薪酬。
薪酬委員會每年至少召開兩次常會。
委員會成員
姓名 |
主要經(學)歷 |
薪酬委員會 |
審計委員會 |
永續及風險管理委員會 |
朱佳真(董事) |
.美國哈佛大學醫療政策與管理 碩士.健亞生物科技(股)公司國際事務處長.健亞生物科技(股)公司新藥開發事業副總經理 |
V |
||
李世仁(獨立董事) |
.美國南加大化學 博士.易威生醫科技(股)公司董事長.浩理生技管理顧問(股)公司董事總經理.合裕管理顧問股份有限公司投資長.Silver Biotech Management, Inc. Managing Director.中華開發工業銀行投資部資深協理 |
V (召集人) |
V |
V |
劉克宜(獨立董事) |
.廈門大學會計 博士.美國伊利諾大學會計 碩士.國立政治大學財稅 學士.會計研究發展基金會審計準則委員會委員.中華民國會計師公會全國聯合會理事 |
V |
V (召集人) |
V |
張金明(獨立董事) |
.美國德州大學奧斯汀分校藥學 博士,國立台灣大學藥學系畢業.美國愛力根公司(Allergan Inc.)藥品,製程、及技術開發高階資深主管.美國禮來藥廠(Eli Lilly & Company)資深研究員 |
V |
V |
V |
委員會運作情形
年度 |
薪酬委員會 |
審計委員會 |
永續及風險管理委員會 |
114年度 |
Download |
Download |
Download |
113年度 |
Download |
Download |
Download |
112年度 |
Download |
Download |
– |
111年度 |
Download |
Download |
– |
110年度 |
Download |
Download |
– |
109年度 |
Download |
Download |
– |
108年度 |
Download |
Download |
– |
107年度 |
Download |
Download |
– |
106年度 |
Download |
Download |
– |
105年度 |
Download |
– | – |
104年度 |
Download |
– | – |
103年度 |
Download |
– | – |
102年度 |
Download |
– | – |
委員會績效評估
年度 |
薪酬委員會 |
審計委員會 |
永續暨風險管理委員會 |
114年度 |
Download |
Download |
Download |
113年度 |
Download |
Download |
– |
112年度 |
Download |
Download |
– |
111年度 |
Download |
Download |
– |
內部稽核之組織及運作
一、內部稽核之目的:
內部稽核的目的,在於評估、檢查內部控制制度之有效性、報導之可靠性、相關法令之遵循,並協助董事會及經理人檢查及覆核內部控制制度之缺失及衡量營運之效果及效率,並適時提供建議,以確保內部控制制度得以持續有效實施及作為檢討修正內部控制制度之依據。
二、內部稽核組織:
本公司設置隸屬於董事會之獨立內部稽核單位,配置內部稽核主管一人,並列席董事會報告稽核業務。
除內部稽核主管之任免,應經審計委員會同意,並提董事會決議,並於董事會通過之次月十日前以網際網路資訊系統向主管機關申報,其餘內部稽核人員之任免、考評及薪酬,依據本公司人力資源管理作業、績效考核辦法及員工酬勞分配辦法等規定,須由稽核主管簽報董事長核定;稽核人員之績效考核方式同一般員工,由個人完成自評後經稽核主管初核,送交董事長覆核決定。
三、內部稽核運作說明:
1.稽核範圍:內部稽核工作包括檢查及評估公司各單位及子公司內部控制制度設計及執行的有效性。
2.稽核對象:稽核對象包括本公司各單位及子公司所負責之所有業務。
3.稽核作業程序:
(1) 每年年底前擬訂次年度稽核計畫,並提報董事會核准後執行。
(2) 執行稽核作業:依董事會核准之年度稽核計畫執行稽核作業,或依本公司董事會、管理階層指示或專案、業務所需,執行特定項目查核。
(3) 自行檢查作業:督促本公司內部各單位及子公司每年辦理內部控制制度自行檢查作業一次,並覆核各單位及子公司之自行檢查報告。
4.稽核報告之呈送與報告:
(1) 稽核報告及追蹤報告陳核後,於稽核項目完成之次月底前交各監察人查閱。
(2) 內部稽核人員執行工作時,如發現重大違規情事或公司有受重大損害之虞,除立即作成報告陳核外並通知各監察人。
(3) 稽核報告若有缺失則請相關單位配合改善。
5.追蹤缺失改善之執行情形:
內部稽核人員對於檢查所發現之內部控制制度之缺失及異常事項,定期作成追蹤報告,以確定相關單位業已採取適當之改善措施。
6.對外申報作業:
依「公開發行公司建立內部控制制度處理準則」之規定期限內,依規定格式以網際網路資訊系統辦理各項應申報備查作業。
|
|
1.公司章程 |
Download |
2.背書保證施行作業程序 |
Download |
3.資金貸與他人作業程序 |
Download |
4.取得或處分資產處理程序(含衍生性商品交易) |
Download |
5.董事會議事規範 |
Download |
6.股東會議事規則 |
Download |
7.董事選任辦法 |
Download |
8.獨立董事之職責範疇規則 |
Download |
9.道德行為準則 |
Download |
10.誠信經營守則 |
Download |
11.薪資報酬委員會組織規程 |
Download |
12.內部重大資訊處理暨防範內線交易管理作業程序 |
Download |
13.檢舉非法與不道德或不誠信行為案件之處理方法 |
Download |
14.誠信經營作業程序及行為指南 |
Download |
15.審計委員會組織規程 |
Download |
16.董事會暨功能性委員會績效評估辦法 |
Download |
17.公司治理實務守則 |
Download |
18.永續發展實務守則 |
Download |
19.風險管理政策與作業程序 |
Download |
20.永續暨風險管理委員會組織規程 |
Download |
發言人:
行政處資深處長:蔣維民 先生
TEL:02-23211978#2631
E-mail:williechiang@genovate-bio.com
代理發言人:
財務副總經理:林惠玲 小姐
TEL:03-5982221#116
E-mail:annlin@genovate-bio.com
股務聯絡人:

 En
En